
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
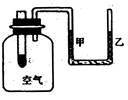
”“ΆΦΈΣΡ≥―ß…ζ…ηΦΤΒΡ“ΜΗω Β―ιΉΑ÷ΟΘ§¥σ ‘Ιή÷–ΉΑ”–Ιΐ―θΜ·ΡΤΙΧΧεΓΘœ÷Άυ¥σ ‘Ιή÷–Φ”»κΥ°Θ§œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «Θ® Θ©
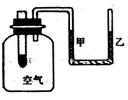 A. ‘Ιή÷–ΖΔ…ζΝΥ÷ΟΜΜΖ¥”Π
A. ‘Ιή÷–ΖΔ…ζΝΥ÷ΟΜΜΖ¥”Π
B.“ΜΕΈ ±ΦδΚσΘ§Ω¥ΒΫΓΑUΓ±–ΈΙή÷–ΒΡ“ΚΟφ”“±Ώ…ΐΗΏΘ§Ήσ±Ώœ¬ΫΒ
C.ΓΑ÷ϋ¥φΓ±‘ΎΖ¥”ΠΈο÷–ΒΡΉήΡήΝΩΒΆ”Ύ…ζ≥…ΈοΒΡΉήΡήΝΩ
D.ΙψΩΎΤΩ÷–ΤχΧεΒΡΖ÷Ή”‘ΎΖ¥”ΠΚσ‘ωΦ”
| AΘ° ‘Ιή÷–ΖΔ…ζΝΥ÷ΟΜΜΖ¥”Π |
| BΘ°“ΜΕΈ ±ΦδΚσΘ§Ω¥ΒΫΓΑUΓ±–ΈΙή÷–ΒΡ“ΚΟφ”“±Ώ…ΐΗΏΘ§Ήσ±Ώœ¬ΫΒ |
| CΘ°ΓΑ÷ϋ¥φΓ±‘ΎΖ¥”ΠΈο÷–ΒΡΉήΡήΝΩΒΆ”Ύ…ζ≥…ΈοΒΡΉήΡήΝΩ |
| DΘ°ΙψΩΎΤΩ÷–ΤχΧεΒΡΖ÷Ή”‘ΎΖ¥”ΠΚσ‘ωΦ” |
|
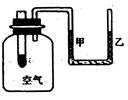
”“ΆΦΈΣΡ≥―ß…ζ…ηΦΤΒΡ“ΜΗω Β―ιΉΑ÷ΟΘ§¥σ ‘Ιή÷–ΉΑ”–Ιΐ―θΜ·ΡΤΙΧΧεΘ°œ÷Άυ¥σ ‘Ιή÷–Φ”»κΥ°Θ§œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «
| |
| [ΓΓΓΓ] | |
AΘ° |
‘Ιή÷–ΖΔ…ζΝΥ÷ΟΜΜΖ¥”Π |
BΘ° |
“ΜΕΈ ±ΦδΚσΘ§Ω¥ΒΫΓΑUΓ±–ΈΙή÷–ΒΡ“ΚΟφ”“±Ώ…ΐΗΏΘ§Ήσ±Ώœ¬ΫΒ |
CΘ° |
ΓΑ÷ϋ¥φΓ±‘ΎΖ¥”ΠΈο÷–ΒΡΉήΡήΝΩΒΆ”Ύ…ζ≥…ΈοΒΡΉήΡήΝΩ |
DΘ° |
ΙψΩΎΤΩ÷–ΤχΧεΒΡΖ÷Ή”‘ΎΖ¥”ΠΚσ‘ωΦ” |
| ||
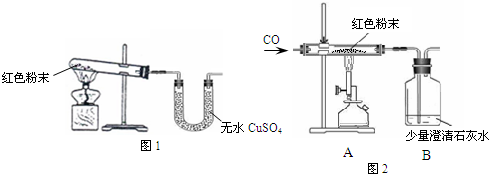
| Ζ¥”Π«Α | Ζ¥”ΠΚσ | |
| Δώ Ήι |
≤ΘΝßΙήΚΆΚλ…ΪΖέΡ©ΒΡΉή÷ ΝΩΈΣ37.3g | ≤ΘΝßΙήΚΆΙΧΧεΈο÷ ΒΡΉή÷ ΝΩΈΣ36.1g |
| Δρ Ήι |
œ¥ΤχΤΩΚΆΥυ Δ»ή“Κ ΒΡΉή÷ ΝΩΈΣ180.0g |
œ¥ΤχΤΩΚΆΤΩ÷–Έο÷ ΒΡΉή÷ ΝΩΈΣ183.1g |
1.A(ΒβΒΞ÷ ”ωΒμΖέ±δάΕ…ΪΘ§Εχ≤Μ «ΒβΥαΦΊ)
2.D(Ά§Έ¬Ά§―Ιœ¬Θ§mgΤχΧεA”κngΤχΧεBΒΡΖ÷Ή” ΐΡΩœύΆ§Θ§ΥΒΟςΈο÷ ΒΡΝΩœύΆ§Θ§AΓΔBΓΔC’ΐ»ΖΘ§DΆ§Έ¬Ά§―Ιœ¬Θ§ΤχΧεA”κΤχΧεBΒΡΟήΕ»÷°±»Β»”ΎΥϋΟ«ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣm ΘΚ n)
3.C(¥”Δέ¥ΠΒΦ≥ωΒΡΤχΧεΚ§”–…ΌΝΩSO2ΓΔO2 ΓΔN2Β»Θ§≤ΜΩ…÷±Ϋ”≈≈»κ¥σΤχΘ§Ζώ‘ρ‘λ≥…Έέ»Ψ)
4.A(Bœν”…”Ύ≤Μ÷ΣΒάΤχΧεΒΡΉ¥Χ§Θ§
5.A(Ζ≈≥ω»»ΝΩΠΛH<0Θ§Υυ“‘A¥μΈσΘΜΤδΥϋΥΒΖ®Ψυ’ΐ»Ζ)
6.A(Υ°ΒΡ»»Έ»Ε®–‘±»ΫœΗΏ «“ρΈΣΥ°Ζ÷Ή”÷–«β―θΦϋΒΡΦϋΡή¥σΘΜΫπ τΨßΧεΒΦΒγ «“ρΈΣΚ§”–Ή‘”…“ΤΕ·ΒΡΒγΉ”ΘΜάκΉ”ΨßΧε”≤Ε»Ϋœ¥σΓΔΡ―”Ύ―ΙΥθ «“ρΈΣάκΉ”ΦϋΦϋΡή¥σ)
7.D (D÷–…œœ¬“ΤΕ· ±Θ§ΝΫΕΥ“ΚΟφ Φ÷’ΤΫΚβΥΒΟςΉΑ÷Ο¬©Τχ)
8.B(Ιΐ―θΜ·ΡΤΙΧΧε”κΥ°Ζ¥”ΠΘ§ «Ζ≈»»Ζ¥”ΠΘ§AΓΔC¥μΈσΘΜΖ≈»» ΙΙψΩΎΤΩ÷–ΤχΧεΈ¬Ε»…ΐΗΏ≈ρ’ΆΘ§‘ρ”“±Ώ…ΐΗΏΉσ±Ώœ¬ΫΒ)
9.A(ClOΘ≠ΘΪ2IΘ≠ΘΪ2HΘΪ===ClΘ≠ΘΪI2ΘΪH2OΘΜSOΘΪI2ΘΪH2O===2IΘ≠ΘΪSOΘΪ2HΘΪΘ§Υυ“‘Ω…÷Σ―θΜ·–‘ΈΣΘΚClOΘ≠>I2>SOΘ§“ρΈΣΔΎ÷–Φ”»κΙΐΝΩΒΡNa2SO3 »ή“ΚΘ§Υυ“‘Δέ÷–Κ§”–BaSO3≥ΝΒμΘΜΔΌ÷–ΝρΥα÷ΜΤπΒΫΥα–‘Ής”ΟΘ§ΔΎ÷ΜΡή÷ΛΟςSO”–ΜΙ‘≠–‘)
10.C(Εΰ‘Σ»θΥα”ΠΖ÷≤ΫΒγάκΘΜ≤ίΥαΒΈΕ®KMnO4 τ”Ύ―θΜ·ΜΙ‘≠ΒΈΕ®Θ§≤Μ”Ο÷Η ΨΦΝΘΜ““ΕΰΥαΆ―Υ°Ζ÷Ϋβ≤ζΈο «COΓΔCO2ΚΆH2O)
11.A((NH4)2SO4ΚΆCH3COOHΟςœ‘ τ”ΎΒγΫβ÷ ΘΜCl2 «ΒΞ÷ Φ»≤Μ τ”ΎΒγΫβ÷ “≤≤Μ τ”ΎΖ«ΒγΫβ÷ ΘΜΥδ»ΜNH3ΒΡΥ°»ή“ΚΡήΙΜΒΦΒγΘ§Ρ« «”…”Ύ…ζ≥…ΝΥ“ΜΥ°ΚœΑ±ΒΡ‘≠“ρΘ§Ι NH3 τ”ΎΖ«ΒγΫβ÷ ΓΘ)
12.D(CsClΚΆNaClΒΡ“θΓΔ―τάκΉ”≈≈Ν–ΖΫ Ϋ≤ΜΆ§ΘΜΫπ τΨßΧε÷–÷Μ”–―τάκΉ”Θ§ΟΜ”–“θάκΉ”ΘΜΖ÷Ή”ΨßΧε÷–≤Μ“ΜΕ®Κ§”–Ι≤ΦέΦϋ»γœΓ”–ΤχΧε)
13.D(ΔΌΥΒΟς”–BrΘ≠ΓΔCOΘ§”–COΨΆΟΜ”–Fe2ΘΪΔΎΥΒΟςΟΜ”–SOΔέΥΒΟςΟΜ”–IΘ≠)
14.D(ΡήΖΔ…ζ’βΝΫΗωΒγΦΪΖ¥”ΠΒΡΩ…Ρή «‘≠Βγ≥ΊΘ§“≤Ω…Ρή «ΒγΫβ≥ΊΘ§»γΙϊ «‘≠Βγ≥ΊΘ§‘ρbΈΣΧζΒγΦΪΘ§aΈΣΟΜΧζΜνΤΟΒΡΫπ τΜρΖ«Ϋπ τΉωΒγΦΪΘ§ΒγΫβ»ή“ΚΈΣΚ§Ά≠άκΉ”ΒΡ»ή“ΚΘΜ»γΙϊ «ΒγΫβ≥ΊΘ§b”ΟΧζΉωΒγΦΪΚΆΒγ‘¥ΒΡ’ΐΦΪœύΝ§Θ§aΩ…“‘ΚΆΧζœύΆ§ΒΡΒγΦΪ“≤Ω…“‘≤ΜΆ§Θ§»ή“ΚΈΣΚ§Ά≠άκΉ”ΒΡ»ή“Κ)
15.C(A≥ΤΝΩ ±”ΠΉσΈο”“¬κΘ§B≈δ÷Τ150mL0.10mol/L»ή“Κ”Π”Ο150mLΒΡ»ίΝΩΤΩΘ§Εχ«““Σ”Ο≤ΘΝßΑτ“ΐΝςΘΜDάδΡΐΥ°ΒΡΖΫœρ”Π¥”œ¬Ϋχ…œ≥ω)
16.D(ΔΌΥυ»Γ≈®ΝρΥαΒΡΧεΜΐ…ΌΘ§ΔΎΔέΔήΨυ‘λ≥…»ή÷ ΒΡΥπ ß)
17.Έ Χβ1ΘΚ(1)Κœ≥…Α±ΙΛ“ΒΓΓΝρΥαΙΛ“Β(ΤδΥϊΚœάμ¥πΑΗ“≤’ΐ»Ζ) (2Ζ÷)
Έ Χβ2ΘΚCuΘΪ4HΘΪΘΪ2NO(≈®)===Cu2ΘΪΘΪ2NO2ΓϋΘΪ2H2O
3CuΘΪ8HΘΪΘΪ2NO(œΓ)===3Cu2ΘΪΘΪ2NOΓϋΘΪ4H2O(ΤδΥϊΚœάμ¥πΑΗ“≤’ΐ»Ζ)(2Ζ÷)
Μ·―ß?ΒΎ“≥(ΦϊΖ¥Οφ)Έ Χβ3ΘΚΖ≈»»ΓΓC(ΫπΗ’ ·ΓΔs)ΘΫC( ·ΡΪΓΔs)ΘΜΠΛHΘΫΘ≠1.90kJ/mol(2Ζ÷)
Έ Χβ4ΘΚ(1)ΒΎΕΰΗωΖ¥”ΠΈΣΘΚAl3ΘΪΘΪ3OHΘ≠===Al(OH)3Γΐ (2Ζ÷)
(2)ΉνΚσ“ΜΗωάκΉ”Ζ¥”ΠΈΣΘΚAl(OH)3ΘΪOHΘ≠===AlOΘΪ2H2O (2Ζ÷)
Έ Χβ5ΘΚ4KMnO4ΘΪ5KIΘΪ7H2SO4===4MnSO4ΘΪI2ΘΪ3KIO3ΘΪ3K2SO4ΘΪ7H2O (2Ζ÷) (ΤδΥϊΚœάμ¥πΑΗ“≤’ΐ»Ζ)
18.(1)ΔΌ2ClΘ≠Θ≠2eΘ≠ΘΫCl2Γϋ(2Ζ÷)ΓΓ”Ο Σ»σΒΡΒμΖέΘ≠KI ‘÷ΫΩΩΫϋYΦΪ÷ßΙήΩΎ(ΤδΥϋΚœάμ¥πΑΗΨυΩ…)(2Ζ÷)
ΔΎ”…”Ύ2HΘΪΘΪ2eΘ≠ΘΫH2ΓϋΓΓΖ≈≥ω«βΤχΘ§ ΙΥ°ΒΡΒγάκΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§ Ιc(OHΘ≠)≤ΜΕœ‘ω¥σΘ§Υυ“‘pHΜα‘ω¥σ(2Ζ÷)
Δέœ»”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§ΦΧΕχ±δ≥…Μ“¬Χ…ΪΘ§ΉνΚσ±δ≥…ΚλΚ÷…Ϊ(2Ζ÷)
(2)ΔΌA(1Ζ÷)ΓΓΔΎB(1Ζ÷)
19.(ΟΩΩ’2Ζ÷)(1)NaIΓΓNaClO
(2)2IΘ≠ΘΪClOΘ≠ΘΪH2O===I2ΘΪClΘ≠ΘΪ2OHΘ≠ΓΓI2ΘΪ5ClOΘ≠ΘΪ2OHΘ≠===2IOΘΪ5ClΘ≠ΘΪH2O
(3)Cl2ΘΪ2NaOH===NaClOΘΪNaClΘΪH2O
20.(1)KClO3 (1Ζ÷)ΓΓH????????H(1Ζ÷)
(2)ΔΌΙΊ±’Ζ÷“Κ¬©ΕΖΜν»ϊΘ§‘ΎII÷–Φ”Υ°Θ§ΟΜΙΐ≥ΛΒΦΙήΩΎΘ§”ΟΨΤΨΪΒΤΈΔ»»‘≤ΒΉ…’ΤΩΘ§»τII÷–”–Τχ≈ίΟΑ≥ωΘ§ΆΘ÷ΙΦ”»»ΚσΘ§”–Υ°Ϋχ»κII÷–ΒΡ≥ΛΒΦΙήΘ§–Έ≥…“ΜΕΈΈ»Ε®ΒΡΥ°÷υΘ§‘ρ÷ΛΟςIΤχΟή–‘ΝΦΚΟΓΘ (Μρ”Ο÷ΙΥ°Φ–Φ–ΉΓc¥ΠΘ§œρΖ÷“Κ¬©ΕΖ÷–Φ”Υ°Θ§¥ρΖ÷“Κ¬©ΕΖΒΡΜν»ϊΘ§»τΖ÷“Κ¬©ΕΖ÷–ΒΡΥ°≤Μ‘Όœ¬ΝςΘ§‘ρ÷ΛΟςIΤχΟή–‘ΝΦΚΟΓΘ)(2Ζ÷)
ΔΎMnO2ΘΪ4HΘΪΘΪ2ClΘ≠Mn2ΘΪΘΪCl2ΓϋΘΪ2H2O(2Ζ÷)
ΔέS2Θ≠ΘΪCl2===SΓΐΘΪ2 ClΘ≠(2Ζ÷)
Μ·―ß?ΒΎ“≥ ΔήIIΓΓIII(1Ζ÷)ΓΓ≥ΐ»Ξ¬»Τχ÷–ΒΡΥ°’τΤχ(ΜρΗ…‘כּΤχ)(1Ζ÷)
(3)Cl2ΘΪH2O2===2HClΘΪO2(2Ζ÷)
21.(1)7Cl2ΘΪ14NaOH===9NaClΘΪ4NaClOΘΪNaClO3ΘΪ7H2O
(2)C(NaCl)ΘΫ1.8mol/LΘ§Cl(NaClO)ΘΫ0.8mol/LΘ§C(NaClO3)ΘΫ0.2mol/LΓΓ(ΟΩΗω2Ζ÷)
ΫβΈωΘΚΫβ¥π¥ΥΧβΒΡΙΊΦϋ «ΒΎ(1)Έ .Ω…ΗυΨίΒΟ ßΒγΉ” ΐœύΒ»»ΖΕ®…ζ≥…ΈοNaClΓΔNaClOΓΔNaClO3ΒΡΈο÷ ΒΡΝΩ÷°±»Θ§ΫχΕχ»ΖΕ®Μ·―ßΖΫ≥Χ Ϋ÷–Μ·―ßΦΤΥψ ΐ.
(1)“άΧβ“βΩ……η…ζ≥…NaClOΒΡΈο÷ ΒΡΝΩΈΣ4molΘ§NaClO3ΒΡΈο÷ ΒΡΝΩΈΣ1molΘ§…η…ζ≥…NaClΒΡΈο÷ ΒΡΝΩxΘ§ΗυΨίΒΟ ßΒγΉ”ΒΡΈο÷ ΒΡΝΩœύΒ»Θ§”–ΘΚ1ΓΝxΘΫ1ΓΝ4molΘΪ5ΓΝ1molΘ§ΫβΒΟΘΚxΘΫ9mol.
NaClΓΔNaClOΓΔNaClO3Μ·―ßΦΤΝΩ ΐ÷°±»”κ…ζ≥…Ε‘”ΠΈο÷ ΒΡΈο÷ ΒΡΝΩœύΒ»Θ§Φ¥Β»”Ύ9ΓΟ4ΓΟ1.Ψί¥ΥΩ…–¥≥ωΉήΒΡΜ·―ßΉ÷ΖΫ≥Χ ΫΘΚ7Cl2ΘΪ14NaOH===9NaClΘΪ4NaClOΘΪNaClO3ΘΪ7H2O
(2)n(Cl2)ΘΫ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com