
题目列表(包括答案和解析)
| 空气成分 | 人体呼出气体成分 | |
| N2 | 78% | 74% |
| O2 | 21% | 16% |
| H2O | 0.5% | 6% |
| CO2 | 0.03% | 4% |
Na2O2曾经是潜水艇或航天器中最理想的供氧剂。下表是人体呼出气体的成分(均为体积百分含最)。
|
|
空气 成分 |
人体呼出 气体成分 |
|
N2 |
78% |
74% |
|
O2 |
21% |
16% |
|
H2O |
0. 5% |
6% |
|
CO2 |
0. 03% |
4% |
(1)已知一个人一天大约要产生16 mol CO2。若全部被Na2O2吸收,需要Na2O2________ g。
(2)若要使被吸收的CO2与产生的O2体积相等,就需
要在Na2O2中添加KO2.计算要达到该目的.Na2O2与KO2的物质的量比例是 。
已知:4KO2+2CO2=2K2CO3+3O2
(3)计算100 L空气经过人体呼吸后,呼出气体中O2的体积(标准状况下,保留2位小数)____ L。
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处 理,无用物质排出航天器。100 L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100 L(可供使用的化学试剂只有Na2O2).通过计算回答:若先利用CO2,还需要利用水蒸气,求需要水蒸气体积 L。
(10分)我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
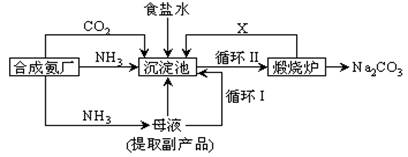
(1) 沉淀池中发生的化学反应方程式是 。
(2) 写出上述流程中X物质的分子式 。
(3) 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是 。
(4)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
(5) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
(6) CO2是制碱工业的重要原料,目前,常用的两种制碱方法中CO2的来源有何不同? 。
一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,它们之间通常形成共价键。请查阅下列化合物中元素的电负性数值,判断它们哪些是共价化合物。
(1)NaF (2)AlCl3 (3)NO (4)MgO (5)BeCl2 (6)CO2
共价化合物____________________________________________________________。
离子化合物____________________________________________________________。
|
元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
电负性 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
|
元素 |
Mg |
N |
Na |
O |
P |
S |
Si |
|
电负性 |
1.2 |
3.0 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com