
题目列表(包括答案和解析)
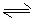 2(t-BuNO) 。
2(t-BuNO) 。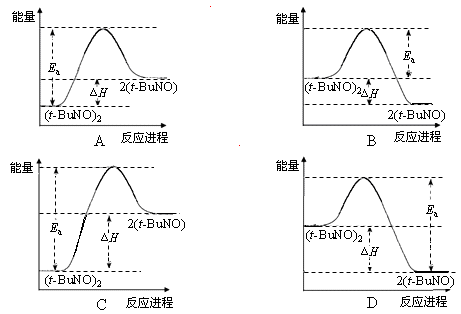
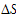 ____ 0(填“>”、“<”或“=”)。在 ________ (填“较高”或“较低”)温度下有利于该反应自发进行。
____ 0(填“>”、“<”或“=”)。在 ________ (填“较高”或“较低”)温度下有利于该反应自发进行。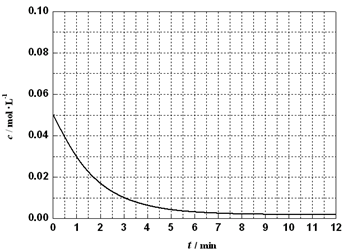
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量 浓度(mol·L-1) | NaOH物质的量 浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,若a 7(填>、<或=),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度![]() (A-)与
(A-)与![]() (Na+)的大小关系是 。
(Na+)的大小关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是 酸(选填“强”或“弱”)。
该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的![]()
![]() = mol·L-1。
= mol·L-1。
(14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
|
实验 编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
|
甲 |
0.2 |
0.2 |
pH=a |
|
乙 |
c |
0.2 |
pH=7 |
|
丙 |
0.2 |
0.1 |
pH>7 |
|
丁 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,用a来说明HA是强酸还是弱酸,若a 7,则HA是强酸;若a 7, 则HA是弱酸(填<、>、=)。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2 (选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是 。
(3)丙组实验结果分析,HA是 酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)= mol·L-1。
| |||||
(8分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验 编号 | HA物质的量 浓度(mol· L-1) | NaOH物质的 量浓度(mol· L-1) | 混合溶液的 pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
| A.前者大 | B.后者大 |
| C.二者相等 | D.无法判断 |
一、选择题(共126分,每小题6分)
1、D 2、B 3、B 4、D 5、B
6、D 7、D 8、C 9、D 10、A 11、A 12、B 13、A
14、D 15、B 16、BD 17、C 18、CD 19、B 20、D 21、C
二、非选择题(共174分)
22、I、如图所示(7分)理科综合.files/image385.jpg)
理科综合.files/image387.gif)
Ⅱ、(1)理科综合.files/image234.gif) ,
,理科综合.files/image390.gif) (4分)
(4分)
(2)连线如图(4分)
(3)BD(2分)
23、(1)根据动能定理有:理科综合.files/image392.gif) (4分)
(4分)
解得:理科综合.files/image394.gif) m (2分)
m (2分)
(2)设小球在作用力区域上方运动的时间是理科综合.files/image396.gif) ,进入作用力区域的速度是
,进入作用力区域的速度是理科综合.files/image211.gif) ,在作用力区域内的加速度是
,在作用力区域内的加速度是理科综合.files/image399.gif) ,运动的时间为
,运动的时间为理科综合.files/image401.gif) ,则有:
,则有:
理科综合.files/image403.gif) s(2分)
s(2分)
理科综合.files/image405.gif) (1分),
(1分),理科综合.files/image407.gif) (1分)
(1分)
理科综合.files/image409.gif) (1分),
(1分), 理科综合.files/image411.gif) (2分)
(2分)
解得:理科综合.files/image413.gif) s(1分)
s(1分)
小球的运动周期 理科综合.files/image415.gif) s(2分)
s(2分)
24、解:(1)以理科综合.files/image417.gif) 组成的系统为研究对象,设第一次
组成的系统为研究对象,设第一次理科综合.files/image227.gif) 与
与理科综合.files/image231.gif) 碰后至
碰后至理科综合.files/image417.gif) 有共同速度
有共同速度理科综合.files/image421.gif) 时,
时,理科综合.files/image229.gif) 在
在理科综合.files/image227.gif) 上相对于
上相对于理科综合.files/image227.gif) 滑行的距离为
滑行的距离为理科综合.files/image426.gif) ,碰撞后
,碰撞后理科综合.files/image417.gif) 组成的系统动量守恒,以向左为正方向,有:
组成的系统动量守恒,以向左为正方向,有:
理科综合.files/image428.gif) (2分)
(2分)
解得:理科综合.files/image421.gif) =2.0m/s,方向向左 (2分)
=2.0m/s,方向向左 (2分)
由能量守恒定律得: 理科综合.files/image431.gif) (2分)
(2分)
解得:理科综合.files/image433.gif) m(1分)
m(1分)
设第二次理科综合.files/image227.gif) 与
与理科综合.files/image231.gif) 碰后至
碰后至理科综合.files/image417.gif) 有共同速度
有共同速度理科综合.files/image437.gif) 时,
时,理科综合.files/image229.gif) 在
在理科综合.files/image227.gif) 上相对于
上相对于理科综合.files/image227.gif) 滑行的距离为
滑行的距离为理科综合.files/image442.gif) ,则有:
,则有:
理科综合.files/image444.gif) (2分)
(2分)
理科综合.files/image446.gif) (2分)
(2分)
解得:理科综合.files/image437.gif) =1.0m/s ,
=1.0m/s ,理科综合.files/image449.gif) m (2分)
m (2分)
若第2次碰撞后理科综合.files/image229.gif) 恰好滑到
恰好滑到理科综合.files/image227.gif) 的最左端,则在
的最左端,则在理科综合.files/image227.gif) 与
与理科综合.files/image231.gif) 发生第3次碰撞时
发生第3次碰撞时理科综合.files/image229.gif) 就以
就以理科综合.files/image437.gif) 的速度滑上
的速度滑上理科综合.files/image231.gif) ,且在
,且在理科综合.files/image231.gif) 上做匀减速运动,所以木板
上做匀减速运动,所以木板理科综合.files/image227.gif) 的长度
的长度理科综合.files/image459.gif) m。(1分)
m。(1分)
(2)根据动能定理得:理科综合.files/image461.gif) (4分)
(4分)
解得:理科综合.files/image463.gif) m(1分)
m(1分)
所以理科综合.files/image229.gif) 在
在理科综合.files/image231.gif) 上滑行的距离
上滑行的距离理科综合.files/image467.gif) m。
m。
25、解:(1)理科综合.files/image318.gif) 粒子在匀强磁场中做匀速圆周运动,由洛伦兹力提供向心力,即有:
粒子在匀强磁场中做匀速圆周运动,由洛伦兹力提供向心力,即有:
理科综合.files/image469.gif) (2分)
(2分)
得:理科综合.files/image471.gif) =0.2m=20cm (2分)
=0.2m=20cm (2分)
(2)设理科综合.files/image310.gif) 与过
与过理科综合.files/image320.gif) 点的水平线交于
点的水平线交于理科综合.files/image475.gif) 点,对于向
点,对于向理科综合.files/image477.gif) 端偏转的
端偏转的理科综合.files/image318.gif) 粒子,当其做圆周运动的轨迹与
粒子,当其做圆周运动的轨迹与理科综合.files/image310.gif) 相切时偏离
相切时偏离理科综合.files/image475.gif) 点最远,设切点为
点最远,设切点为理科综合.files/image246.gif) ,对应的圆心为
,对应的圆心为理科综合.files/image482.gif) ,如图所示,则由几何关系得:
,如图所示,则由几何关系得:
理科综合.files/image484.gif) =16cm (2分)
=16cm (2分)
对于向理科综合.files/image335.gif) 端偏转的
端偏转的理科综合.files/image318.gif) 粒子,当沿
粒子,当沿理科综合.files/image487.gif) 方向射入时,偏离
方向射入时,偏离理科综合.files/image475.gif) 点最远,
点最远,
理科综合.files/image490.jpg) 设此时其做圆周运动的轨迹与
设此时其做圆周运动的轨迹与理科综合.files/image310.gif) 交于
交于理科综合.files/image493.gif) 点,对应的圆心为
点,对应的圆心为理科综合.files/image062.gif)
(如图所示),则由几何关系得:
理科综合.files/image496.gif) cm
cm
故金箔理科综合.files/image310.gif) 被
被理科综合.files/image318.gif) 粒子射中区域的长度为:
粒子射中区域的长度为:
理科综合.files/image499.gif) =32cm。 (2分)
=32cm。 (2分)
(3)设从理科综合.files/image493.gif) 点穿出的
点穿出的理科综合.files/image318.gif) 粒子的速度为
粒子的速度为理科综合.files/image502.gif) ,因
,因
理科综合.files/image504.gif) =0.6,所以
=0.6,所以理科综合.files/image506.gif) (1分)
(1分)
即理科综合.files/image502.gif) 的方向与电场
的方向与电场理科综合.files/image240.gif) 方向垂直,故穿出的
方向垂直,故穿出的理科综合.files/image318.gif) 粒子在电场中做类平抛运动,其轨迹如上图所示。
粒子在电场中做类平抛运动,其轨迹如上图所示。
沿速度理科综合.files/image502.gif) 的方向
的方向理科综合.files/image318.gif) 粒子做匀速直线运动,故有:位移
粒子做匀速直线运动,故有:位移 理科综合.files/image509.gif) cm (1分)
cm (1分)
沿电场理科综合.files/image240.gif) 的方向
的方向理科综合.files/image318.gif) 粒子做匀加速直线运动,故有:位移
粒子做匀加速直线运动,故有:位移理科综合.files/image511.gif) cm (1分)
cm (1分)
则由 理科综合.files/image513.gif) (1分)
(1分) 理科综合.files/image515.gif) (1分)
(1分) 理科综合.files/image517.gif) (1分)
(1分)
解得:理科综合.files/image519.gif) m/s (2分)
m/s (2分)
故此理科综合.files/image318.gif) 粒子从金箔上穿出时,损失的动能为:
粒子从金箔上穿出时,损失的动能为:
理科综合.files/image521.jpg)
理科综合.files/image523.gif) (2分)
(2分)
理科综合.files/image525.jpg) 26、(15分)
26、(15分)
理科综合.files/image527.jpg)
理科综合.files/image529.jpg)
27、(17分)(1)无明显现象;红色褪去;先变红后褪色;变蓝色(各1分)
(2)理科综合.files/image531.gif) (2分)
(2分)
(3)①理科综合.files/image533.gif) (2分)
(2分)
②A(2分)
(4)①B(2分)
②负(1分);理科综合.files/image535.gif) (2分)
(2分)
③0.25(2分)
28、(15分)(1)理科综合.files/image537.gif) (2分)
(2分)
(2)①O ②理科综合.files/image539.gif) (各2分)
(各2分)
(3)①理科综合.files/image541.gif) (2分) ②
(2分) ②理科综合.files/image543.gif) (3分)
(3分)
(4)①理科综合.files/image545.gif) ②
②理科综合.files/image547.gif) (各2分)
(各2分)
29、(13分)(1)10:1 理科综合.files/image549.gif) mol 或
mol 或理科综合.files/image551.gif) mol (各3分)
mol (各3分)
(2)2 0.28理科综合.files/image553.gif)
解析:(1)因为理科综合.files/image555.gif) ,
, 理科综合.files/image557.gif) 溶液的
溶液的理科综合.files/image559.gif) , 即
, 即理科综合.files/image561.gif) mol?L-1
mol?L-1 理科综合.files/image563.gif) 溶液的
溶液的理科综合.files/image565.gif) , 即
, 即理科综合.files/image567.gif) mol?L-1
mol?L-1
所以理科综合.files/image569.gif) 又因为
又因为理科综合.files/image571.gif)
所以用理科综合.files/image573.gif) 计算沉淀的物质的量
计算沉淀的物质的量 理科综合.files/image575.gif)
用理科综合.files/image577.gif) 计算沉淀的物质的量
计算沉淀的物质的量 理科综合.files/image579.gif)
所以生成沉淀的物质的量为理科综合.files/image581.gif) 或
或理科综合.files/image583.gif) 。
。
(2)令理科综合.files/image585.gif) ,
,理科综合.files/image587.gif) 则
则
理科综合.files/image589.gif)
理科综合.files/image591.gif) (3分)
(3分)
又因为 理科综合.files/image593.gif) ;
;
所以理科综合.files/image595.gif) 。(4分)
。(4分)
30、(共21分,每空3分)
(1)理科综合.files/image010.gif) ;
;
(2)黑藻利用瓶中0.1%的理科综合.files/image377.gif) 溶液提供的
溶液提供的理科综合.files/image010.gif) 进行光合作用,产生
进行光合作用,产生理科综合.files/image062.gif) 使瓶内气压增加,
使瓶内气压增加,
将水从导管排出,并推动U形管中的水柱下降和上升,单位时间内液面差值即为光合速率。
(3)I、①新鲜黑藻茎段量、添加的各种化学成分等(至少是黑藻量和0.1%理科综合.files/image377.gif) 溶液量)
溶液量)
③将甲乙两装置放在光照强度相同的条件下培养;
④分别测量甲乙的U形玻璃管两边的液面差(下降和上升的高度和);
Ⅱ、验证温度对黑藻光合作用的影响或探究黑藻光合作用的最适温度;
(4)细胞质流动;
31、(共21分,第一小题每空3分,其余每空2分)
(1)雄; 非编码区和内含子; 碱基对(脱氧核苷酸排列顺序或遗传信息)。
(2)翅长;非同源;F1中长翅个体相互交配产生的子代中(F2)短翅只有雄性、与性别有关
(3)①常染色体 ;X;
②理科综合.files/image599.gif) 、
、理科综合.files/image601.gif) 、
、理科综合.files/image603.gif) 、
、理科综合.files/image605.gif)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com