
题目列表(包括答案和解析)
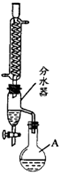 (2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
(2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:| 实验编号 | 实验记录 | |
| (3)验证鳔内含有氧气 | 将燃着的木条放入集气瓶中 | 木条能继续燃烧,证明含有氧气 |
| (4)验证鳔内含二氧化碳 | 操作方法: |
实验现象: 该反应的离子方程式是: 该实验中能否使用上述(3)实验结束后集气瓶中剩余的气体,为什么? |
| (5)分离出氮气 | 取一份装在100mL医用注射器中的鳔内气体进行分离:第一步,将气体通过 过 |
第三步实验时还可以选用 |
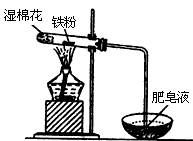
铁是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是 。
(2)某实验小组利用右图装置验证铁与水蒸气的反应。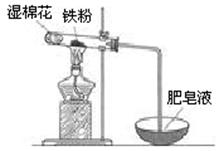
①湿棉花的作用是 ,试管中反应的化学方程式是 。
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是 (填序号)。
a.一定有Fe2+、H+和Fe3+ b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有 H+ d.一定有Fe3+、H+,可能有Fe2+
(3)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
①铁与浓硫酸反应的化学方程式是 。
②气体中混有CO2的原因是(用化学方程式表示) 。
③将672 mL(标准状况)收集到的气体通入足量溴水中,发生反应:
SO2 + Br2 + 2H2O =" 2HBr" + H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66 g。由此推知收集到的气体中SO2的体积分数是 。
铁是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是 。
(2)某实验小组利用右图装置验证铁与水蒸气的反应。
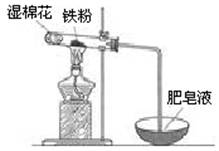
①湿棉花的作用是 ,试管中反应的化学方程式是 。
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是 (填序号)。
a.一定有Fe2+、H+和Fe3+ b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有 H+ d.一定有Fe3+、H+,可能有Fe2+
(3)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
① 铁与浓硫酸反应的化学方程式是 。
② 气体中混有CO2的原因是(用化学方程式表示) 。
③ 将672 mL(标准状况)收集到的气体通入足量溴水中,发生反应:
SO2 + Br2 + 2H2O = 2HBr + H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66 g。由此推知收集到的气体中SO2的体积分数是 。
第I卷 选择题
1.A 2.C 3.B 4.C 5.B 6. C 7.B 8.A 9. D 10. C 11. A 12.C 13.B
14. C 15 .A 16.B 17.ACD 18. BC 19.B 20. BD 21. AD
第II卷 非选择题
 22 I 0.590 2.642
22 I 0.590 2.642
每空2分,共4分。
Ⅱ(1)E;C
(2)甲
(3)连接实物图
(4)①变大 ②10Ω
(1)每空1分(2)3分(3)4分(4)每空2分。
23.
(1)由小物块上滑过程的速度―时间图线,可知: (3分)
(3分)
 m/s2
(1分)
m/s2
(1分)
小物块冲上斜面过程中加速度的大小为
(2)小物块受重力、支持力、摩擦力,沿斜面建立直角坐标系,
 (2分)
(2分)
 (2分)
(2分)
 (2分)
(2分)
代入数据解得  (2分)
(2分)
(3)设物块冲上斜面所能达到的最高点距斜面底端距离为s,
向上运动阶 (3分)
(3分) (1分)
(1分)
24.解:小车在半径为R的圆周上作圆周运动,处于圆周轨道的最高点时,小车和人所受重力之和提供向心力,设小车滑行到D点时的速度为u,根据牛顿第二定律
 (4分)
(4分)
得u= m
m
设人和小车以共同速度v ,从水平面运动到D的过程中机械能守恒,根据机械能守恒定律得
 (4分)
(4分)
v=15m/s (2分)
在人接触小车,并使小车和人一起前进的过程中,无水平方向外力作用,故水平方向上动量守恒,得
 (4分)
(4分)
v0=20m/s (3分)
25.(1)质子射入磁场后做匀速圆周运动,有
evB=mv2/r (3分)
可得v=eBr/m (1分)
(2)质子沿x轴正向射入磁场后经1/4圆弧后以速度v垂直于电场方向进入电场,周期为
 (2分)
(2分)
在磁场中运动的时间
t1=T/4=πm/2eB (1分)
进入电场后做抛物线运动,沿电场方向运动r后到达y轴,因此有
 (1分)
(1分)
t2= (1分)
(1分)
所求时间为t=
t1+ t2=
 (1分)
(1分)
(3)质子在磁场中转过120°角后从P点垂直电场线进入电场,如图所示。
P点距y轴的距离
x1=r+rsin30°=1.5r  (2分)
(2分)
因此可得质子从进入电场至到达y轴所需时间为
 =
= (2分)
(2分)
质子在电场中沿y轴方向做匀速直线运动,因此有
 (2分)
(2分)
 质子到达y轴的位置坐标为
质子到达y轴的位置坐标为 即(0,r+
即(0,r+ ) (2分)
) (2分)
图 (2分)
26.(10分)(1)N2 (2分)
 |
(2) (2分,如写出CO正确的电子式也给分)
(3)离子键、非极性键。(2分,第二空答共价键也给分) ②④ (2分,答案全正确给分)
(4)CS2+2H2O CO2+2H2S(2分)
CO2+2H2S(2分)
27.(18分)(1)Al+4OH-?3e- = AlO2-+2H2O(2分)
(2)10-2?10-12 mol/L, 或c(OH-)?c(H+) (2分) < (2分)
(3)否(1分);因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解(2分)。
 |
(4)4NH3+5O2 4NO+6H2O (2分,条件错误扣1分)
|