
题目列表(包括答案和解析)

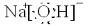
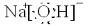
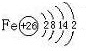
| ||
| ||
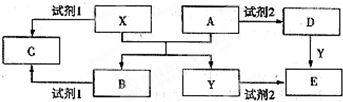
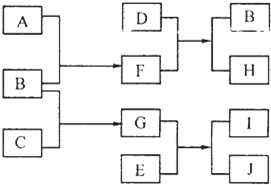 A、B、C、D、E是中学化学常见的单质,其中A、C常温下为气态,B、D、E是金属.E的摩尔质量是A的2倍,F、G、H、I、J五种化合物分别由组成上述五种单质中的两种元素组成.D与F反应放出大量的热.它们之间的转化关系如图所示(反应条件已省略);
A、B、C、D、E是中学化学常见的单质,其中A、C常温下为气态,B、D、E是金属.E的摩尔质量是A的2倍,F、G、H、I、J五种化合物分别由组成上述五种单质中的两种元素组成.D与F反应放出大量的热.它们之间的转化关系如图所示(反应条件已省略);A+B![]() C+D B+E=2D?
C+D B+E=2D?
(1)写出A的电子式______________。?
(2)写出B的化学式______________。?
(3)写出D的电子式______________。
(1)写出A的电子式:______________,E的电子式:______________。
(2)B的化学式为______________,C的化学式为______________,D的化学式为______________,E的化学式为______________。
(3)用电子式表示D的形成过程:____________________________________________________。
选择题(本题包括8小题。每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分,共48分。)
题号
14
15
16
17
18
19
20
21
答案
A
C
BC
B
AD
A
ACD
BD
非选择题
22(共18分)
(1)D
 (2)A、1.010
(2)A、1.010
B、①如图所示(4分)

② 见图(4分)
③  ,I1、I2分别为电流表A1、A2的读数,r2为电流表A2的内阻。(4分)
,I1、I2分别为电流表A1、A2的读数,r2为电流表A2的内阻。(4分)
23.(16分)(1)设月球表面的重力加速度为g,小球从h高处下落到月球表面的时间为t,有
h=gt2/2 ① (2分)
L=v0t ② (2分)
由以上两式解得:g=2hv02/L2 ③ (2分)
绕月球表面飞行的卫星的发射速度近似等于卫星的环绕速度,有
mv2/R=mg ④ (2分)
由③④解得:v= (2分)
(2分)
(2)由向心力公式有GMm/R2=mg ⑤ (2分)
又ρ=M/V,V=4πR3/3 ⑥ (2分)
由③⑤⑥式解得:ρ=3hv02/(2πGRL2) ⑦ (2分)
24.(18分)解(1)金属棒未进入磁场,电路总电阻 ① (2分)
① (2分)
回路中感应电动势为: V ②
(2分)
V ②
(2分)
灯炮中的电流强度为: A
③ (2分)
A
③ (2分)
(2)因灯泡亮度不变,故在 s末金属棒刚好进入磁场,且做匀速运动,
s末金属棒刚好进入磁场,且做匀速运动,
此时金属棒中的电流强度: A
④ (2分)
A
④ (2分)
恒力大小: N
⑤ (2分)
N
⑤ (2分)
(3)因灯泡亮度不变,金属棒产生的感应电动势为:
 V ⑥ (2分)
V ⑥ (2分)
金属棒在磁场中的速度: m/s
⑦ (2分)
m/s
⑦ (2分)
金属棒未进入磁场的加速度为: m/s2
⑧ (2分)
m/s2
⑧ (2分)
金属棒的质量: kg
⑨ (2分)
kg
⑨ (2分)
25、(20分)解:(1)粒子自P点进入磁场,从O1点水平飞出磁场,运动的半径必为b,则
 ①(2分)
①(2分)
解得  ②(2分)
②(2分)
(2)粒子自O1点进入电场,最后恰好从N板的边缘平行飞出,设运动时间为t,则
2R=v0t ③(2分)
t=nT(n=1,2,…) ④(2分)

 ⑤(4分)
⑤(4分)
解得  (n=1,2,…) ⑥(2分)
(n=1,2,…) ⑥(2分)
 (n=1,2,…) ⑦(2分)
(n=1,2,…) ⑦(2分)
(3)当t=粒子以速度v0沿O2O1射入电场时,则该粒子恰好从M板边缘以平行于极板的
速度射入磁场,且进入磁场的速度仍为v0,运动的轨道半径仍为R. ⑧(2分)
设进入磁场的点为Q,离开磁场的点为O4,圆心为O3,如图所示,四边形OQ O3O4是菱形,故O O4∥ QO3. 所以P、O、O4三点共线,即PO O4为圆的直径.即P O4间的距离为2R.
⑨(2分)
雅礼中学第六次月考化学试题参考答案
6.【解析】 两溶液中离子数目的差别在于水电离出来的H+的不同,由于HCN比HF更难电离,故CN-的水解程度比F-的大,NaCN溶液中OH-离子浓度要大些,反过来溶液中由水电离出来的H+离子浓度小。
【答案】 B
7.【解析】 由于碳酸钡与胃酸能反应生成可溶性的钡盐导致人体中毒,实际使用的是硫酸钡;不同活泼程度的金属铰接在一起,有可能形成原电池而加速金属的腐蚀;酒精一般采用体积分数来表示,而不是质量分数。
【答案】 D
8.【解析】 电镀时镀件作阴极,镀层金属材料作阳极;由于连通电路后,C电极附近溶液变红,说明该处溶液产生了OH-,水电离出来的H+发生了放电,发生了还原反应,应连接电源的负极;故a为电源的正极,e为阳极,发生氧化反应。
【答案】B
9.【解析】由于正向是个气体物质的量增大的方向,随着反应的发生,容器中气体物质的量增大,A容器的体积增大,压强不变,B容器压强增大,体积不变,故B容器的压强比A容器的2倍还要大;B容器的反应速率快。
X(g)+Y(g) 2Z(g)+W(g)
2Z(g)+W(g)
初: 1 1 0 0
平衡:1-x 1-x 2x x
A容器的体积之比等于气体物质的量之比,可以得出x=0.8;A容器中X的转化率为80%;由于增大压强,平衡朝逆方向进行,所以B容器中Y的体积分数要比A容器的大。
【答案】 C
10.【解析】 由于碳原子数目比较多,可见分子中的对称性比较好;如果分子结构为
(CH3)
【答案】 C
11.【解析】 可以由同系列的系列差-CH=CH-直接计算
【答案】B
12.【解析】 分子中共有6个碳原子,又由于该酯的一种水解产物经催化氧化可转化成它的另一种水解产物,可见形成酯的酸部分和醇部分均有三个碳原子,且醇要能最终氧化为酸,故醇羟基的位置只能在端基,应为丙醇(CH3CH2CH2OH),对应的酸为丙酸(CH3CH2COOH)。
【答案】D
13.【解析】长期盛放NaOH溶液的滴瓶不易打开,是由于玻璃的成分中有SiO2,与NaOH溶液反应生成少量的Na2SiO3溶液,Na2SiO3是一种矿物胶,能将试剂瓶的瓶子与塞子粘连在一起而打不开。
【答案】B
26.(每空两分,共18分)
(1) Cl2+H2O=H++Cl-+HClO (方程式可以写等号,也可用可逆符号) ;
2Fe2++Cl2=2Fe3++2Cl-
(2)CH4+Cl2 CH3Cl+HCl CH3Cl+Cl2
CH3Cl+HCl CH3Cl+Cl2 CH2Cl2+HCl
CH2Cl2+HCl
CH2Cl2+Cl2 CHCl3+HCl 或CH4+3Cl2
CHCl3+HCl 或CH4+3Cl2
 CHCl3+3HCl ; 取代;大于
CHCl3+3HCl ; 取代;大于
(3)O3 ;极性分子
(4)不能 ;在酸性条件下,Cl-能被ClO3-氧化成Cl2,因而不能制得ClO2。
或ClO3-+5Cl-+6H+=3Cl2↑+3H3O(没有写方程式,只有文字理由也可以给分)
27.(每空2分,共12分)
(1)Cl2
(2)3NO2+H2O=2HNO3+NO;
(3)4NH3+6NO 5N2+6H2O;
5N2+6H2O;
(4)14
(5)< ;在溶液中NH4NO3电离出的NH4+会发生水解:
NH4++H2O NH3?H2O+H+,导致溶液呈酸性,故溶液的pH<7。
NH3?H2O+H+,导致溶液呈酸性,故溶液的pH<7。
28.(每空2分,共16分)
(1)Br
 (2)醛基
(或-CHO)和羧基(-COOH)(对1个给1分,共2分); 4步
; 取代反应(或水解反应)
(2)醛基
(或-CHO)和羧基(-COOH)(对1个给1分,共2分); 4步
; 取代反应(或水解反应)
(3)
(4)①2CH3OH+O2 2HCHO+2H2O
2HCHO+2H2O
② +3NaOH
2NaBr +CH3OH+
+3NaOH
2NaBr +CH3OH+ 
 +H2O(注意加热条件、配平、小分子等的规范)
+H2O(注意加热条件、配平、小分子等的规范)
③HCOOH+2Ag(NH3)2OH (NH4)2CO3+2Ag↓+2NH3↑+H2O(氧化产物写成CO2、H2CO3或NH4HCO3、HOCOONH4均可以)
(NH4)2CO3+2Ag↓+2NH3↑+H2O(氧化产物写成CO2、H2CO3或NH4HCO3、HOCOONH4均可以)
29.(每空2分,共14分)
(1)-COOH、―OH;(也可以答羧基、羟基)(对1个给1分,共2分)
(2)4
(3)4种
(4)第一组:A  C
C  ;
;
第二组:A  C
C 
从满足成六元环酯的要求看,变换两个取代基上的碳原子的数目和位置关系,还有两种结构也符合要求。
雅礼中学第六次月考生物试题参考答案
1.B 2.B 3.D 4.A 5.C
30.(本大题满分为24分)
Ⅰ.(每一空2分,共10分)
(1)① 青毛:白毛大致等于1:1
② b1 >b3>b2 >b4
③ b3> b1 >b2 >b4
(2) Bb4
(3)选用多只褐毛雌兔与该黑毛雄兔交配,若后代均为黑毛兔,则该黑毛雄兔的基因型为b3b3,若后代出现了褐毛兔,则该黑毛兔的基因型为b3b4
Ⅱ.(第1小题每一空1分,其余小题每一空2分,共14分)
(1)酶的合成 代谢过程
(2)hhDD和HHdd 叶片内含氰∶叶片不含氰=9∶7
(3)
① ddHH或ddHh;
② 向该提取液中加入含氰糖苷,反应物中不能提取氰,而加入氰酸酶后,反应物中能提取到氰 DDhh或Ddhh
③ 向该提取液中分别加入含氰糖苷和氰酸酶,反应物中都不能提取到氰。
31.(第4小问的⑥和⑦每一空2分,其余每一空2分,共18分)
(1)① B
②基因重组 继承了双亲细胞的遗传物质。
(2)③基因工程 工程菌
④通过发酵获得的大量的微生物菌体。
(3)不能合成高丝氨酸脱氢酶
(4)⑤筛选到能高效降解化合物A的细菌 化合物A 异养需氧型
⑥减少 增加
⑦定期取样 细菌数目的对数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com