
题目列表(包括答案和解析)

Ⅰ
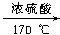
Ⅱ
(1)装置A中发生反应的化学方程式为__________________________________________。
(2)分液漏斗中盛有液体,但打开分液漏斗的活塞时液体不能顺利流下,可能的原因是___
____________________________________________________________________。
(3)装置X的作用是贮存气体,X中广口瓶内应盛放的液体最好是__________。
①Na2CO3溶液 ②酸性高锰酸钾溶液 ③Na2SO4溶液 ④饱和NaHSO3溶液
(4)装置Y、Z中产生的现象相同,但原因不同,Y中是由于(写离子方程式)____________
__________________________________,而Z中则是由于SO2具有_______________。
(5)实验需要收集多瓶二氧化硫气体,在更换集气瓶时,为了减少二氧化硫逸散到空气中,将图Ⅰ中的B部分更换为图Ⅱ所示装置,可以用a、b集气瓶交替收集二氧化硫气体,请回答:
①检查集气瓶b是否漏气的方法是__________________________________________。
②若只用集气瓶a收集气体,在装置气密性良好,并加入药品后,准备制取并收集二氧化硫气体,下一步的操作是________________________________________________。
(6)①若用A装置作为实验室制取乙烯的发生装置,应对A装置作何改进?
____________________________________________________________________
____________________________________________________________________。
②烧瓶中应加入碎瓷片,目的是__________________________________________________。
③写出实验室制取乙烯的化学方程式:____________________________________________。


 CO↑+H2O 请根据以下各装置进行选择组成一套相对较为合理的实验装置图(某些装置可重复使用)
CO↑+H2O 请根据以下各装置进行选择组成一套相对较为合理的实验装置图(某些装置可重复使用) 
1(16分) 某化学兴趣小组利用下图I探究铜和浓 H2SO4 反应生成气体的性质,图II用来收集多瓶该气体,请回答下列问题。(已知:Cu +2H2SO4(浓)![]() CuSO4 + 2H2O + SO2↑)
CuSO4 + 2H2O + SO2↑)

(1) 分液漏斗中盛有浓H2SO4,点燃酒精灯前打开分液漏斗的活塞,浓H2SO4不能顺利流下,可能的原因是________________________________________________。
(2) 装置X的作用是贮存气体,X中广口瓶内应盛放的液体最好是 ;
① Na2CO3 溶液 ② 酸性高锰酸钾 ③ Na2SO3 溶液 ④ 饱和NaHSO3 溶液
(3) 装置Y中产生的现象是 ,请用方程式解释产生该现象的原因 。
(4) 装置Z中产生的现象是 ,请用简要文字解释产生该现象的原因 。(提示:硝酸具有强氧化性)
(5) 实验需要收集多瓶反应产生的气体,在更换集气瓶时,为了减少气体逸散到空气中,将图I中的B部分更换为图II所示装置,可以用a、b 集气瓶交替收集二氧化硫气体,请回答:
① 检查集气瓶b 是否漏气的方法是______________________________________________________。
② 若只用集气瓶a 收集气体,在装置气密性良好,并加入药品后,准备制备并收集二氧化硫气体,下一步的操作是 。
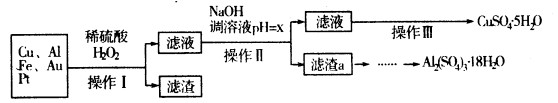
下图是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:
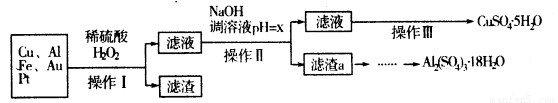
已知下列信息:
Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
开始沉淀 | 1.1 | 4.0 | 5.4 |
完全沉淀 | 3.2 | 5.2 | 6.7 |
请回答下列问题:
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式:????????????? .。
(2)在操作Ⅱ中,x的取值范围是???????????? ? 。
(3)在操作Ⅲ中,蒸发浓缩需要的玻璃仪器有??????????? 。
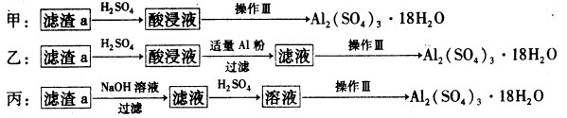
(4)由滤渣a制取Al2(SO4)3·l8H2O,探究小组设计了三种方案:
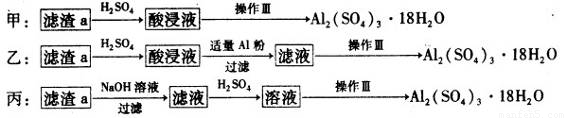
综合考虑上述三种方案,最具可行性的是?????? (填序号)。
(5)为测定CuSO4·5H2O晶体的纯度,进行下列实验:取a g试样配成l00 mL溶液,每次取20.00mL,消除干扰离子后,用b mol·L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00 mL。(常温时,5%的Na2H2Y水溶液,其pH为4—6。)
①CuSO4·5H2O晶体的纯度是 ?????????? 。
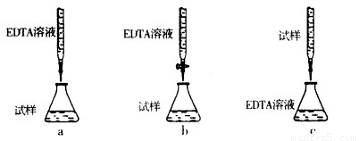
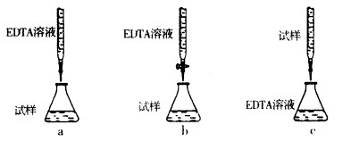
②下列滴定方式中,最合理的是(夹持部分略去) ??????????? (填序号)。
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |
一、选择题答案。(每小题3分,共48分)
1―8 CDCBDBCA 9―16 BADCAABC

二、非选择题答案。(52分)
17.(7分)(1) (2分) (2)
(3)CD (2分)
(2分) (2)
(3)CD (2分)
 18.(共18分)
18.(共18分)
(1)H C(每个1分,共3分)
(2)C (1分) (3) (4)1 (2分)
(5)① (2分)
(2分)
②促进(1分)。  (2分)
③ab(3分)
(2分)
③ab(3分)
(6) 或其他合理答案(3分)
或其他合理答案(3分)
19.(14分)(1)10 (2分);
11(2分)
(2分);
11(2分)
(2) (2分);(写出后者即给2分)
(2分);(写出后者即给2分)
 (2分)
(2分)
(3) 1:9 (3分)
(4)a+b=13(3分)
20.(13分)(1) (2分)
(2分)
(2)分液漏斗上口的塞子未打开(或漏斗未与大气相通或漏斗塞子的凹槽未与颈部的通气孔对准(1分)
(3)④(2分) (4)
(5)①关闭K ,在烧杯中用水封住玻璃导管口,用手捂住集气瓶b,烧杯用导管口有气泡产生,松手后,导管内有一段液柱保持不降则气密性好(3分)
,在烧杯中用水封住玻璃导管口,用手捂住集气瓶b,烧杯用导管口有气泡产生,松手后,导管内有一段液柱保持不降则气密性好(3分)
②打开K ,关闭K
,关闭K ,点燃酒精灯。(2分)
,点燃酒精灯。(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com