
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
Θ®8Ζ÷Θ©Ρ≥Μ·―ß–Υ»Λ–ΓΉι“ΣΆξ≥…÷–ΚΆ»»ΒΡ≤βΕ®ΓΘ
Θ®1Θ© Β―ιΉά…œ±Η”–…’±≠Θ®¥σΓΔ–ΓΝΫΗω…’±≠Θ©ΓΔ≈ίΡ≠ΥήΝœΓΔ≈ίΡ≠ΥήΝœΑεΓΔΫΚΆΖΒΈΙήΓΔΜΖ–Έ≤ΘΝßΑτΓΔ0.5molΓΛ L-1 ―ΈΥαΓΔ0.55molΓΛ L-1NaOH»ή“ΚΘ§…–»±…ΌΒΡ Β―ι≤ΘΝß”ΟΤΖ « ΓΔ ΓΘ
Θ®2Θ©ΥϊΟ«Φ«¬ΦΒΡ Β―ι ΐΨί»γœ¬ΘΚ
| Β ―ι ”Ο ΤΖ | »ή “Κ Έ¬ Ε» | ÷–ΚΆ»»ΓςH | |||
| t1 | t2 | ||||
| ΔΌ | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20Γφ | 23.3Γφ |
|
| ΔΎ | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20Γφ | 23.5Γφ |
“―÷ΣΘΚQ=Cm(t2 -t1)Θ§Ζ¥”ΠΚσ»ή“ΚΒΡ±»»»»ίCΈΣ4.18KJΓΛΓφ-1ΓΛ Kg-1Θ§ΗςΈο÷ ΒΡΟήΕ»ΨυΈΣ1gΓΛcm-3ΓΘ
ΦΤΥψΆξ≥……œ±μΓΘΓςH=
Θ®3Θ©Ρ≥―–ΨΩ–ΓΉιΫΪV1 mL 1.0 mol/L HCl»ή“ΚΚΆV2 mLΈ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΜλΚœΨυ‘»Κσ≤βΝΩ≤ΔΦ«¬Φ»ή“ΚΈ¬Ε»Θ§ Β―ιΫαΙϊ»γœ¬ΆΦΥυ Ψ( Β―ι÷– Φ÷’±Θ≥÷V1ΘΪV2ΘΫ50 mL)ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
―–ΨΩ–ΓΉιΉωΗΟ Β―ι ±ΜΖΨ≥Έ¬Ε» (ΧνΓΑΗΏ”ΎΓ±ΓΔΓΑΒΆ”ΎΓ±ΜρΓΑΒ»”ΎΓ±)22 ΓφΘ§¥ΥΖ¥”ΠΥυ”ΟNaOH»ή“ΚΒΡ≈®Ε»”ΠΈΣ mol/LΓΘ
Ρ≥―–ΨΩ–ΓΉιΫΪV1 mL 1.0 mol/L HCl»ή“ΚΚΆV2 mLΈ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΜλΚœΨυ‘»Κσ≤βΝΩ≤ΔΦ«¬Φ»ή“ΚΈ¬Ε»Θ§ Β―ιΫαΙϊ»γœ¬ΆΦΥυ Ψ( Β―ι÷– Φ÷’±Θ≥÷V1ΘΪV2ΘΫ50 mL)ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©―–ΨΩ–ΓΉιΉωΗΟ Β―ι ±ΜΖΨ≥Έ¬Ε» (ΧνΓΑΗΏ”ΎΓ±ΓΔ ΓΑΒΆ”ΎΓ±ΜρΓΑΒ»”ΎΓ±)22 Γφ.
(2)”…ΧβΗ…ΦΑΆΦ–ΈΩ…÷ΣΘ§V1©UV2= ±Θ§ΥαΦν«ΓΚΟΆξ»Ϊ÷–ΚΆΘ§¥ΥΖ¥”ΠΥυ”ΟNaOH»ή“ΚΒΡ≈®Ε»”ΠΈΣ mol/LΓΘ
Θ®3Θ© Β―ι ±ΫΪΥαΦν‘ΎΦρ“ΉΝΩ»»ΦΤ÷–ΜλΚœΘ§≤Δ”Ο ΫΝΑηΘ§ Ι»ή“ΚΜλΚœΨυ‘»ΓΘΨ≠”–ΙΊΦΤΥψ
÷Σ¥ΥΖ¥”ΠΙ≤Ζ≈≥ωQ kJΒΡ»»ΝΩΘ§«κ–¥≥ω¥ΥΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
Θ®12Ζ÷Θ©Ρ≥―–ΨΩ–ΓΉιΫΪV1 mL 1.0 mol/L HCl»ή“ΚΚΆV2 mLΈ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΜλΚœΨυ‘»Κσ≤βΝΩ≤ΔΦ«¬Φ»ή“ΚΈ¬Ε»Θ§ Β―ιΫαΙϊ»γœ¬ΆΦΥυ Ψ( Β―ι÷– Φ÷’±Θ≥÷V1ΘΪV2ΘΫ50 mL)ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
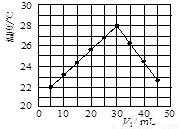
Θ®1Θ©―–ΨΩ–ΓΉιΉωΗΟ Β―ι ±ΜΖΨ≥Έ¬Ε» (ΧνΓΑΗΏ”ΎΓ±ΓΔ
ΓΑΒΆ”ΎΓ±ΜρΓΑΒ»”ΎΓ±)22 ΓφΘ§≈–ΕœΒΡ“άΨί « ΓΘ
(2)”…ΧβΗ…ΦΑΆΦ–ΈΩ…÷ΣΘ§V1©UV2= ±Θ§ΥαΦν«ΓΚΟΆξ»Ϊ÷–ΚΆΘ§¥ΥΖ¥”ΠΥυ”ΟNaOH»ή“ΚΒΡ≈®Ε»”ΠΈΣ mol/LΓΘ
Θ®3Θ© Β―ι ±ΫΪΥαΦν‘ΎΦρ“ΉΝΩ»»ΦΤ÷–ΜλΚœΘ§≤Δ”Ο ΫΝΑηΘ§ Ι»ή“ΚΜλΚœΨυ‘»ΓΘΨ≠”–ΙΊΦΤΥψ÷Σ¥ΥΖ¥”ΠΙ≤Ζ≈≥ωQ kJΒΡ»»ΝΩΘ§«κ–¥≥ω¥ΥΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
Θ®8Ζ÷Θ©”Ο“ΜΕ®≈®Ε»ΒΡœΓ―ΈΥα”κœΓNaOH»ή“Κ‘ΎΉσœ¬ΆΦΥυ ΨΒΡΉΑ÷Ο÷–Ϋχ––÷–ΚΆΖ¥”ΠΘ§Ά®Ιΐ≤βΕ®Ζ¥”ΠΙΐ≥Χ÷–ΥυΖ≈≥ωΒΡ»»ΝΩΩ…ΦΤΥψ÷–ΚΆ»»ΓΘ“―÷Σ«ΩΥα”κ«ΩΦνΒΡ÷–ΚΆ»»ΈΣ57.3KJ/molΘ§Υ°ΒΡ±»»»»ίΈΣ4.2J/(gΓΛΓφ)Θ§”–ΙΊ»»ΝΩ”κ±»»»»ίΒΡΦΤΥψΙΪ ΫΘΚQ=mΓΝcΓΝΓςtΘ®QΈΣ»»ΝΩΘ§mΈΣΈο÷ ΒΡ÷ ΝΩΘ§cΈΣ±»»»»ίΘ§ΓςtΈο÷ Έ¬Ε»ΒΡ±δΜ·÷ΒΘ©
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©¥” Β―ιΉΑ÷Ο…œΩ¥Θ§ΆΦ÷–…–»±…ΌΒΡ“Μ÷÷≤ΘΝß”ΟΤΖ «ΘΚ
Θ®2Θ©ΫΪV1 mL 1.0 mol/L HCl»ή“ΚΚΆV2 mLΈ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΜλΚœΨυ‘»Κσ≤βΝΩ≤ΔΦ«¬Φ»ή“ΚΈ¬Ε»Θ§ Β―ιΫαΙϊ»γΆΦΥυ Ψ( Β―ι÷– Φ÷’±Θ≥÷V1ΘΪV2ΘΫ50 mL)ΓΘ
œ¬Ν––π ω’ΐ»ΖΒΡ «
| AΘ°ΉωΗΟ Β―ι ±ΜΖΨ≥Έ¬Ε»ΈΣ22 Γφ | BΘ°ΗΟ Β―ι±μΟςΜ·―ßΡήΩ…“‘ΉΣΜ·ΈΣ»»Ρή |
| CΘ°NaOH»ή“ΚΒΡ≈®Ε»‘Φ «1.00 mol/L | DΘ°ΗΟ Β―ι±μΟς”–Υ°…ζ≥…ΒΡΖ¥”ΠΕΦ «Ζ≈»»Ζ¥”Π |
Θ®12Ζ÷Θ©Ρ≥―–ΨΩ–ΓΉιΫΪV1 mL 1.0 mol/L HCl»ή“ΚΚΆV2 mLΈ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΜλΚœΨυ‘»Κσ≤βΝΩ≤ΔΦ«¬Φ»ή“ΚΈ¬Ε»Θ§ Β―ιΫαΙϊ»γœ¬ΆΦΥυ Ψ( Β―ι÷– Φ÷’±Θ≥÷V1ΘΪV2ΘΫ50 mL)ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ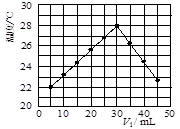
Θ®1Θ©―–ΨΩ–ΓΉιΉωΗΟ Β―ι ±ΜΖΨ≥Έ¬Ε» (ΧνΓΑΗΏ”ΎΓ±ΓΔ
ΓΑΒΆ”ΎΓ±ΜρΓΑΒ»”ΎΓ±)22 ΓφΘ§≈–ΕœΒΡ“άΨί « ΓΘ
(2)”…ΧβΗ…ΦΑΆΦ–ΈΩ…÷ΣΘ§V1©UV2= ±Θ§ΥαΦν«ΓΚΟΆξ»Ϊ÷–ΚΆΘ§¥ΥΖ¥”ΠΥυ”ΟNaOH»ή“ΚΒΡ≈®Ε»”ΠΈΣ mol/LΓΘ
Θ®3Θ© Β―ι ±ΫΪΥαΦν‘ΎΦρ“ΉΝΩ»»ΦΤ÷–ΜλΚœΘ§≤Δ”Ο ΫΝΑηΘ§ Ι»ή“ΚΜλΚœΨυ‘»ΓΘΨ≠”–ΙΊΦΤΥψ÷Σ¥ΥΖ¥”ΠΙ≤Ζ≈≥ωQ kJΒΡ»»ΝΩΘ§«κ–¥≥ω¥ΥΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com