“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO
2是目前大气中含量最高的一种温室气体.因此,控制和治理CO
2是解决“温室效应”的有效途径.
(1)其中一种途径是将CO
2转化成有机物实现碳循环.如:
2CO
2(g)+2H
2O(l)═C
2H
4(g)+3O
2(g)△H=+1411.0kJ/mol
2CO
2(g)+3H
2O(l)═C
2H
5OH(1)+3O
2(g)△H=+1366.8kJ/mol
则由乙烯水化制乙醇反应的热化学方程式为______.
温度(K)
(2)在一定条件下,6H
2(g)+2CO
2(g)

CH
3CH
2OH(g)+3H
2O(g).
CO2转化率(%)
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
根据上表中数据分析:
①温度一定时,提高氢碳比[n(H
2)/n(CO
2)],CO
2的转化率______(填“增大”“减小”“不变”).
②该反应的正反应为______(填“吸”或“放”)热反应.
(3)一定条件下,将3molH
2和1molCO
2两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3H
2(g)+CO
2(g)

CH
3OH(g)+H
2O(g).2min末该反应达到平衡,测得CH
3OH的浓度为0.2mol/L.下列判断不正确的是______.
a.该条件下此反应的化学平衡常数表达式为

b.H
2的平均反应速率为0.3mol/
c.CO
2的转化率为60%
d.若混合气体的密度不再改变时,该反应一定达到平衡状态
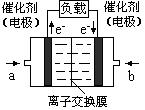
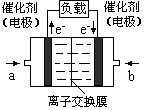
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是______(填“乙醇”或“氧气”),b处电极上发生的电极反应是:______.
(5)CO
2在自然界循环时可与CaCO
3反应,CaCO
3是一种难溶物质,其Ksp=2.8×10
-9.CaCl
2溶液与Na
2CO
3溶液混合可形成CaCO
3沉淀,现将等体积的CaCl
2溶液与Na
2CO
3溶液混合,若Na
2CO
3溶液的浓度为2×10
-4mo1/L,则生成沉淀所需CaCl
2溶液的最小浓度为大于______.


 CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。  CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。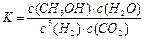
 CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。  CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
 CH3CH2OH(g)+3H2O(g).
CH3CH2OH(g)+3H2O(g). CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.
CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.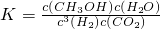 b.H2的平均反应速率为0.3mol/(L?s)
b.H2的平均反应速率为0.3mol/(L?s) 氧气”),b处电极上发生的电极反应是:______.
氧气”),b处电极上发生的电极反应是:______. CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.
CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______. b.H2的平均反应速率为0.3mol/
b.H2的平均反应速率为0.3mol/
 CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.
CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______. b.H2的平均反应速率为0.3mol/
b.H2的平均反应速率为0.3mol/