
题目列表(包括答案和解析)
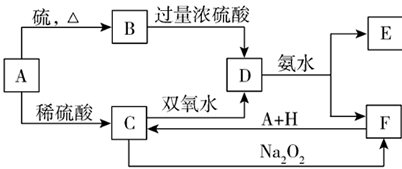

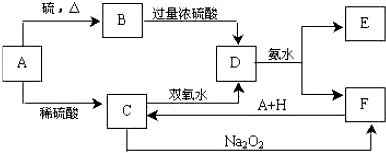

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:________________。
(2)A、B、H的化学式:A________、B________、H________。
(3)①H2O2分子的电子式:________________。
②写出C的酸性溶液与双氧水反应的离子方程式:
_____________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:___________________________________________________________________
_____________________________________________________________________。
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
_____________________________________________________________________。
第I卷
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
A
B
B
C
C
B
B
B
A
B
D
13.(8分)
(1)①非极性 二氧化碳电子式略。 (各1分)
② C(s) + O2(g) = CO2(g) △H = -393.6kJ/mol 2分
(2) ① Al3+ + 4OH- = AlO2- + 2H2O 2分
② Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓ 2分
14.(10分)
. (1)1nm~100nm(1分)
(2)Fe FeS
H2SO4(稀)(3分)
(3)①H H(1分)
H(1分)
②2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
(4)取少量E于试管中,用胶头滴管入NaOH溶液,加热试管,可观察到试管口处
湿润的红色石蕊试纸变蓝。(或其他合理答案)(3分)
15、(8分)
(1)K= (2分) 放热 (1分)
(2)b (1分) 1.5×10-3mol?L-1?s-1 (2分)
(3)bc (1分) (4)c (1分)
16、(10分)
方案一 (1) 保证NaHCO3全部分解 (1分)
方案二
(2)①检查装置的气密性(1分) 硫酸 (1分)
防止空气中水蒸气、CO2进入C管被吸收(1分)
② C (1分)
③需设计一将A、B中的CO2全部吹入C中吸收的气体装置(1分)
方案三
(3)①玻璃棒(1分)
②取少量滤液,再滴加BaCl2少许,如无白色沉淀说明沉淀完全(1分)
③ 51%(2分)
17.(18分)
(1)加成反应 (还原反应)(1分);
(2) CH3COOH 1分
 Br2CH― ―OOCCH3 ; 2分
Br2CH― ―OOCCH3 ; 2分
|