
题目列表(包括答案和解析)
(12分).某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
⑴方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是____________。
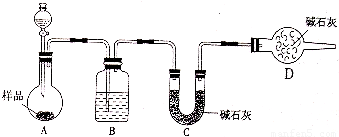
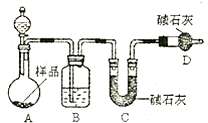
⑵方案二:按下图装置进行实验。并回答以下问题。

①实验前先_____________________。分液漏斗中应该装_____(盐酸或硫酸)。D装置的作用是______________________________________。
②实验中除称量样品质量外,还需称__________________装置前后质量的变化。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是 _______________________________________________。
⑶方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯,漏斗外还用到的玻璃仪器有_______________。
②实验中判断沉淀是否完全的方法是____________________________。
③如加入试剂改为氢氧化钡,已知称得样品10.5g,干燥的沉淀质量为19.7g,测样品中碳酸钠的质量分数为____________。
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.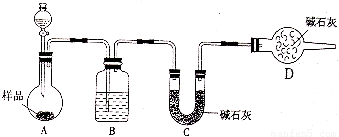
第I卷
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
A
B
B
C
C
B
B
B
A
B
D
13.(8分)
(1)①非极性 二氧化碳电子式略。 (各1分)
② C(s) + O2(g) = CO2(g) △H = -393.6kJ/mol 2分
(2) ① Al3+ + 4OH- = AlO2- + 2H2O 2分
② Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓ 2分
14.(10分)
. (1)1nm~100nm(1分)
(2)Fe FeS
H2SO4(稀)(3分)
(3)①H H(1分)
H(1分)
②2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
(4)取少量E于试管中,用胶头滴管入NaOH溶液,加热试管,可观察到试管口处
湿润的红色石蕊试纸变蓝。(或其他合理答案)(3分)
15、(8分)
(1)K= (2分) 放热 (1分)
(2)b (1分) 1.5×10-3mol?L-1?s-1 (2分)
(3)bc (1分) (4)c (1分)
16、(10分)
方案一 (1) 保证NaHCO3全部分解 (1分)
方案二
(2)①检查装置的气密性(1分) 硫酸 (1分)
防止空气中水蒸气、CO2进入C管被吸收(1分)
② C (1分)
③需设计一将A、B中的CO2全部吹入C中吸收的气体装置(1分)
方案三
(3)①玻璃棒(1分)
②取少量滤液,再滴加BaCl2少许,如无白色沉淀说明沉淀完全(1分)
③ 51%(2分)
17.(18分)
(1)加成反应 (还原反应)(1分);
(2) CH3COOH 1分
 Br2CH― ―OOCCH3 ; 2分
Br2CH― ―OOCCH3 ; 2分
|