
题目列表(包括答案和解析)
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
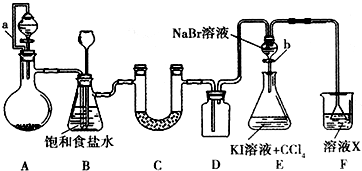 某同学设计如图所示的实验方案,请回答下列问题.
某同学设计如图所示的实验方案,请回答下列问题.下列事实,不能说明氯元素的非金属性比硫元素强的是
A.氯气比硫单质更易与氢气反应 B.HClO4酸性比H2SO4强
C.盐酸是强酸,氢硫酸是弱酸 D.受热时,氯化氢比硫化氢稳定
(13分)A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):

(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是 ;D与Y反应的离子方程式为;
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是 ;D与Y反应的离子方程式为可能为
;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显 (填酸或碱)性,原因是
(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是 ;
D→E的化学反应方程式为 。
【解析】(1)根据图中的转化特点可知,C和强碱反应生成物D还能溶解在强碱中,常见的是铝的化合物的转化,再结合A是金属可知,A是铝和盐酸的÷生成氢气和氯化铝,所以D是氢氧化铝,E是偏铝酸钠。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com