
题目列表(包括答案和解析)
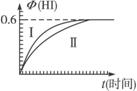
(1)达平衡时,I2(g)的物质的量浓度为______________mol·L-1。
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线(Ⅰ)所示,则该条件可能是_________________(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2 L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应达平衡时,HI的体积分数仍为0.60,则a、b、c的关系为______________(用一个含a、b、c的代数式表示)。
(4)室温时将0.01 mol HI气体溶于水配成100 ml 溶液,则该溶液中由水电离产生的氢离子的物质的量浓度为____________mol·L-1;若降低温度该溶液的pH将____________(填增大、减小或不变)。
14.2g Cl2 含 个氯气分子、 摩尔氯原子,标准状况下所占的体积为 升,与这些Cl2分子数相同的H2的质量是 g ,它们恰好完全反应后得到的氯化氢气体的物质的量是 摩尔,质量为 g,在标准状况下是 升,将产生的氯化氢气体溶于490.4 mL 水中,则所得溶液的质量为 g ,若所得溶液的密度为1.01 g?cm-3 ,则该溶液的体积为 L。 溶液的物质的量浓度为 mol?L-1 ,质量分数为 。
(10分)根据碘与氢气反应的热化学方程式,下列判断正确的是
① I2(g)+H2(g)2HI(g) △H=-9.48 kJ/mol
② I2(s)+H2(g)2HI(g) △H=+26.48 kJ/mol
(1)写出固态碘生成气态碘的热化学方程式: 。
(2)若反应②吸收52.96kJ热量时,转移电子的物质的量是 mol。
(3)对于在恒温、恒容密闭容器中进行的反应①,能说明其达到化学平衡状态的是 。
A. 容器中气体压强不变
B. 容器中气体密度不变
C. 容器中气体颜色的深浅不变
D. 有n个H—H键断裂的同时有2n个H—I键断裂
(4)可通过反应2NO+O2=2NO2和NO2+2H++2I-=NO+I2+H2O来制取碘,NO在制碘过程中的作用是 。
(5)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,采用以下方案:如下图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液的蓝色消失时,立即关闭活塞A。
①用碘水测定SO2的含量的化学方程式是 。
②洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是 。
③洗气瓶C中溶液的蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
(10分)根据碘与氢气反应的热化学方程式,下列判断正确的是
① I2(g)+H2(g) 2HI(g)△H=-9.48 kJ/mol
2HI(g)△H=-9.48 kJ/mol
② I2(s)+H2(g) 2HI(g)△H=+26.48 kJ/mol
2HI(g)△H=+26.48 kJ/mol
(1)写出固态碘生成气态碘的热化学方程式: 。
(2)若反应②吸收52.96kJ热量时,转移电子的物质的量是 mol。
(3)对于在恒温、恒容密闭容器中进行的反应①,能说明其达到化学平衡状态的是 。
A. 容器中气体压强不变
B. 容器中气体密度不变
C. 容器中气体颜色的深浅不变
D. 有n个H—H键断裂的同时有2n个H—I键断裂
(4)可通过反应2NO+O2=2NO2和NO2+2H++2I-=NO+I2+H2O来制取碘,NO在制碘过程中的作用是 。
(5)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,采用以下方案:如下图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液的蓝色消失时,立即关闭活塞A。
①用碘水测定SO2的含量的化学方程式是 。
②洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是 。
③洗气瓶C中溶液的蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
(10分)根据碘与氢气反应的热化学方程式,下列判断正确的是
① I2(g)+H2(g) 2HI(g) △H=-9.48 kJ/mol
2HI(g) △H=-9.48 kJ/mol
② I2(s)+H2(g) 2HI(g) △H=+26.48 kJ/mol
2HI(g) △H=+26.48 kJ/mol
(1)写出固态碘生成气态碘的热化学方程式: 。
(2)若反应②吸收52.96kJ热量时,转移电子的物质的量是 mol。
(3)对于在恒温、恒容密闭容器中进行的反应①,能说明其达到化学平衡状态的是 。
A. 容器中气体压强不变
B. 容器中气体密度不变
C. 容器中气体颜色的深浅不变
D. 有n个H—H键断裂的同时有2n个H—I键断裂
(4)可通过反应2NO+O2=2NO2和NO2+2H++2I-=NO+I2+H2O来制取碘,NO在制碘过程中的作用是 。
(5)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,采用以下方案:如下图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液的蓝色消失时,立即关闭活塞A。

①用碘水测定SO2的含量的化学方程式是 。
②洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是 。
③洗气瓶C中溶液的蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com