
题目列表(包括答案和解析)
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,标况) | 1.12 | 2.24 | 3.36 | 4.48 |

| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
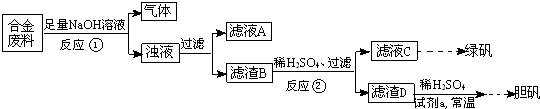
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用。

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和____(填化学式)。
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为____;滤渣D、稀硫酸和试剂a总反应的化学方程式为 。
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加 。
Na2SiO3溶液与过量的CO2反应的离子方程式为 。
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
|
实验编号 |
① |
② |
③ |
④ |
|
稀HNO3体积(mL) |
100 |
200 |
300 |
400 |
|
剩余金属质量(g) |
9.0 |
4.8 |
0 |
0 |
|
NO体积(L,标况) |
1.12 |
2.24 |
3.36 |
4.48 |
①实验①最先溶解的金属发生反应的化学方程式是 。
②滤渣B中Fe的质量分数为____%(精确到0.1%)。

| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |

| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | ||
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
一、1.D?
2.解析:Cl2被完全吸收,Cl2应在下部生成,推知b为正极,a为负极。?
答案:B?
3.C 4.CD 5.B 6.A 7.A 8.BD 9.A?
二、10.(1)Fe Fe-2e-===Fe2+ (2)BC?
(3)隔离空气,防止生成的Fe(OH)2被氧化 加热c,以除去溶解的O2?
(4)BC?
(5)白色沉淀迅速变成灰绿色,最后变成红褐色?
11.(1)有红色物质析出为负极 (2)铜导线变粗为负极?
12.(1)2Cl--2e-===Cl2↑ 升高?
(2)Ca2++CO ===CaCO3↓?
===CaCO3↓?
Mg2++2OH-===Mg(OH)2↓?
(3)AC (4)BC (5)蒸发 过滤?
(6)NaCl+H2O NaClO+H2↑(或2NaCl+2H2O
NaClO+H2↑(或2NaCl+2H2O 2NaOH+H2↑+Cl2↑?
2NaOH+H2↑+Cl2↑?
Cl2+2NaOH===NaCl+NaClO+H2O)?
13.(1)B (2)C?
(3)5KI+KIO3+6HCl===6KCl+3I2+3H2O 5∶1 溶液变蓝?
(4)阳极:I-+3H2O-6e-===IO-3+6H+?
阴极:6H2O+6e-===3H2↑+6OH-?
(5)0.837?
14.T介于
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com