
题目列表(包括答案和解析)
已知:
CH3 (CH2 )2CH3 ( g )+13/2O2 ( g ) =4CO2 ( g ) + 5 H2O ( l );△H=-2878kJ·mol一1
(CH3)2CHCH3 ( g ) +13/2O2 ( g ) =4CO2 ( g ) + 5 H2O ( l );△H = -2869 kJ·mol一1
下列说法正确的是( )
A.等量的异丁烷分子中碳氢键比正丁烷的多
B.正丁烷分子所具有的能量小于异丁烷分子
C.正丁烷的燃烧热(△H )为一2878kJ·mol一1
D.异丁烷转化为正丁烷的过程是一个放热过程
已知:
CH3 (CH2 )2CH3 ( g )+13/2O2 ( g ) =4CO2 ( g ) + 5 H2O ( l );△H=-2878kJ·mol一1
(CH3)2CHCH3 ( g ) +13/2O2 ( g ) =4CO2 ( g ) + 5 H2O ( l );△H = -2869 kJ·mol一1
下列说法正确的是( )
| A.等量的异丁烷分子中碳氢键比正丁烷的多 |
| B.正丁烷分子所具有的能量小于异丁烷分子 |
| C.正丁烷的燃烧热(△H)为一2878kJ·mol一1 |
| D.异丁烷转化为正丁烷的过程是一个放热过程 |
| 13 |
| 2 |
| 13 |
| 2 |
(18分)(1)I.短周期某主族元素M的电离能情况如右图(A)所示。则M元素位于周期表的第 族。
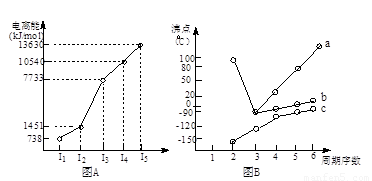
II.图B折线c可以表达出第 族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”)
III.部分有机物的熔沸点见下表:
|
烃 |
CH4 |
CH3CH3 |
CH3(CH2)2CH3 |
硝基苯酚 |
|
|
|
|
沸点/℃ |
-164 |
-88.6 |
-0.5 |
熔点/℃ |
45 |
96 |
114 |
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):
,
。
(2)COCl2俗称光气,分子中C原子采取 杂化成键;其中碳氧原子之间共价键含有
________(填字母):
a.2个σ键;b.2个π键;c.1个σ键.1个π键。
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为 ;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为 。
6B 7C 8D 9C 10B 11B 12A 13D
26 . ( 16 分)( 1 )第三(1 分)IA ( 1 分) ( 2 ) Na > N > H ( 2 分)
( 3 )正四面体结构(l 分)极性共价键(1 分)极性(1 分)
C2A2的电子式: ( 2 分)
( 2 分)

( 2 )防止碳酸钠液体倒吸,便于乙酸乙酯流出 ( 2 分)
( 3 ) I 98 %的浓硫酸具有强氧化性,使部分反应物炭化 ( 2 分)

II ① ② ③ (2 分,答一个且正确得1 分,有错不得分)10 mol?L一1 ( 2 分)
III 能(1 分)因为酯化反应的催化剂是H+,盐酸也能电离出H+ (2 分)
说明:1.本试卷中其它合理答案,可参照此评分标准酌情给分。
2.方程式未写条件或条件不完全、不写“↓”或“↑”均扣一分,不配平不得分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com