
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
ΧΦΥαΡΤΓΣΙΐ―θΜ·«βΦ”ΚœΈο(aNa2CO3ΓΛbH2O2)ΨΏ”–Τ·ΑΉΓΔ…±ΨζΉς”ΟΓΘ Β―ι “”ΟΓΑ¥ΦΈωΖ®Γ±÷Τ±ΗΗΟΈο÷ ΒΡ Β―ι≤Ϋ÷η»γœ¬ΘΚ
ΒΎ1≤ΫΘΚ»Γ ΝΩΧΦΥαΡΤ»ήΫβ”Ύ“ΜΕ®ΝΩΥ°άοΘ§ΒΙ»κ…’ΤΩ÷–ΘΜ‘ΌΦ”»κ…ΌΝΩΈ»Ε®ΦΝ(MgCl2ΚΆNa2SiO3)Θ§ΫΝΑηΨυ‘»ΓΘ
ΒΎ2≤ΫΘΚΫΪ ΝΩ30%ΒΡH2O2»ή“Κ‘ΎΫΝΑηΉ¥Χ§œ¬ΒΈ»κ…’ΤΩ÷–Θ§”Ύ15 ΓφΉσ”“Ζ¥”Π1 hΓΘ
ΒΎ3≤ΫΘΚΖ¥”ΠΆξ±œΚσ‘ΌΦ”»κ ΝΩΈόΥ°““¥ΦΘ§Ψ≤÷ΟΓΔΫαΨßΘ§Ιΐ¬ΥΓΔΗ…‘οΒΟ≤ζΤΖΓΘ
(1)ΒΎ1≤Ϋ÷–Θ§Έ»Ε®ΦΝ”κΥ°Ζ¥”Π…ζ≥…ΝΫ÷÷≥ΘΦϊΒΡΡ―»ήΈοΘ§ΤδΜ·―ßΖΫ≥Χ ΫΈΣ___________________________________________________________ΓΘ
(2)ΒΎ2≤Ϋ÷–Θ§Ζ¥”Π±Θ≥÷ΈΣ15 ΓφΉσ”“Ω…≤…»ΓΒΡ¥κ © «_____________________
___________________________________________________ΓΘ
(3)ΒΎ3≤Ϋ÷–Θ§ΈόΥ°““¥ΦΒΡΉς”Ο «____________________________________ΓΘ
(4)H2O2ΒΡΚ§ΝΩΩ…ΚβΝΩ≤ζΤΖΒΡ”≈Ν”ΓΘœ÷≥Τ»Γm g(‘Φ0.5 g)―υΤΖΘ§”Ο–¬÷σΖ–ΙΐΒΡ’τΝσΥ°≈δ÷Τ≥…250 mL»ή“ΚΘ§»Γ25.0 mL”ΎΉΕ–ΈΤΩ÷–Θ§œ»”ΟœΓΝρΥαΥαΜ·Θ§‘Ό”Οc molΓΛLΘ≠1 KMnO4»ή“ΚΒΈΕ®÷Ν÷’ΒψΓΘ
ΔΌ≈δ÷Τ250 mL»ή“ΚΥυ–ηΒΡ≤ΘΝß“«Τς”–…’±≠ΓΔ≤ΘΝßΑτΓΔΝΩΆ≤________ΓΔ________ΘΜ
ΔΎΒΈΕ®÷’ΒψΙέ≤λΒΫΒΡœ÷œσ «______________________________________ΓΘ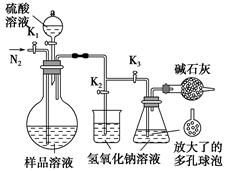
(5)Ω…ΡΘΡβ”Ο’τΝσΖ®≤βΕ®―υΤΖ÷–ΧΦΥαΡΤΒΡΚ§ΝΩΓΘΉΑ÷Ο»γ”“ΆΦΥυ Ψ(Φ”»»ΚΆΙΧΕ®ΉΑ÷Ο“―¬‘»Ξ)Θ§ Β―ι≤Ϋ÷η»γœ¬ΘΚ
≤Ϋ÷η1ΘΚΑ¥”“ΆΦΥυ ΨΉιΉΑ“«ΤςΘ§Φλ≤ιΉΑ÷ΟΤχΟή–‘ΓΘ
≤Ϋ÷η2ΘΚΉΦ»ΖΝΩ»Γ(4)÷–Υυ≈δ»ή“Κ50 mL”Ύ…’ΤΩ÷–ΓΘ
≤Ϋ÷η3ΘΚΉΦ»ΖΝΩ»Γ40.00 mL‘Φ0.2 molΓΛLΘ≠1 NaOH»ή“ΚΝΫΖίΘ§Ζ÷±πΉΔ»κ…’±≠ΚΆΉΕ–ΈΤΩ÷–ΓΘ
≤Ϋ÷η4ΘΚ¥ρΩΣΜν»ϊK1ΓΔK2Θ§ΙΊ±’Μν»ϊK3ΜΚΜΚΆ®»κΒΣΤχ“ΜΕΈ ±ΦδΚσΘ§ΙΊ±’K1ΓΔK2Θ§¥ρΩΣK3ΘΜΨ≠Ζ÷“Κ¬©ΕΖœρ…’ΤΩ÷–Φ”»κ10 mL 3 molΓΛLΘ≠1ΝρΥα»ή“ΚΓΘ
≤Ϋ÷η5ΘΚΦ”»»÷Ν…’ΤΩ÷–ΒΡ“ΚΧεΖ–ΧΎΘ§’τΝσΘ§≤Δ±Θ≥÷“ΜΕΈ ±ΦδΓΘ
≤Ϋ÷η6ΘΚΨ≠K1‘ΌΜΚΜΚΆ®»κΒΣΤχ“ΜΕΈ ±ΦδΓΘ
≤Ϋ÷η7ΘΚœρΉΕ–ΈΤΩ÷–Φ”»κΥαΦν÷Η ΨΦΝΘ§”Οc1 molΓΛLΘ≠1 H2SO4±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§œϊΚΡH2SO4±ξΉΦ»ή“ΚV1 mLΓΘ
≤Ϋ÷η8ΘΚΫΪ Β―ι≤Ϋ÷η1ΓΪ7÷ΊΗ¥ΝΫ¥ΈΓΘ
ΔΌ≤Ϋ÷η3÷–Θ§ΉΦ»Ζ“Τ»Γ40.00 mL NaOH»ή“ΚΥυ–η“Σ Ι”ΟΒΡ“«Τς «________ΘΜ
ΔΎ≤Ϋ÷η1ΓΪ7÷–Θ§»Ζ±Θ…ζ≥…ΒΡΕΰ―θΜ·ΧΦ±Μ«β―θΜ·ΡΤ»ή“ΚΆξ»ΪΈϋ ’ΒΡ Β―ι≤Ϋ÷η «________(Χν–ρΚ≈)ΘΜ
ΔέΈΣΜώΒΟ―υΤΖ÷–ΧΦΥαΡΤΒΡΚ§ΝΩΘ§ΜΙ–η≤Ι≥δΒΡ Β―ι «______________________ΓΘ
Θ®4Ζ÷Θ©¬ΝΓΔΧζΝΫ÷÷Ϋπ τΒΡΒΞ÷ ΦΑΤδΜ·ΚœΈο‘Ύ…ζ≤ζΓΔ…ζΜν÷–”–Ή≈ΙψΖΚΒΡ”Π”ΟΓΘ«κΜΊ¥πΘΚ
Θ®1Θ©ΝΫ÷÷Ϋπ τ”κœΓ―ΈΥαΖ¥”ΠΘ§≥ΐΕΦ…ζ≥…«βΤχΆβΘ§ΜΙΖ÷±π…ζ≥…ΒΡΈο÷ «
_ ___ΓΔ__ __Θ®ΧνΜ·―ß ΫΘ©ΓΘ
Θ®2Θ©ΫΪ±ΞΚΆ¬»Μ·Χζ»ή“ΚΒΈ»κΖ–Υ°÷–Θ§ΒΟΒΫFe(OH)3 ΫΚΧεΓΘΒ±Ιβ χΆ®Ιΐœ¬Ν–Έο÷ ±Θ§ΡήΙέ≤λΒΫΕΓ
¥οΕϊ–ß”ΠΒΡ «__ __Θ®Χν–ρΚ≈Θ©ΓΘ
ΔΌ¬»Μ·Χζ»ή“Κ ΔΎ Fe(OH)3 ΫΚΧε
Θ®3Θ©œρ Δ”–«β―θΜ·¬Ν–ϋΉ«“ΚΒΡ ‘Ιή÷–ΒΈΦ”«β―θΜ·ΡΤ»ή“ΚΘ§ΒΟΒΫΈό…ΪΆΗΟς»ή“ΚΘ§ΗΟΖ¥”ΠΒΡάκΉ”ΖΫ
≥Χ ΫΈΣ ΓΘ
| Β―ι≤Ϋ÷η | Β―ιΫα¬έ |
| Θ®1Θ©≥Τ»ΓA 4.5gΘ§Φ”»» ΙΤδΤϊΜ·Θ§≤βΤδΟήΕ» «œύΆ§ΧθΦΰœ¬H2ΒΡ45±ΕΘ° | Θ®1Θ©AΒΡœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ 90 90 |
| Θ®2Θ©ΫΪ¥Υ4.5gA‘ΎΉψΝΩO2÷–≥δΖ÷»Φ…’Θ§≤Δ ΙΤδ≤ζΈο“ά¥ΈΜΚΜΚΆ®Ιΐ Δ”–ΉψΝΩ≈®ΝρΥαΓΔ«β―θΜ·ΡΤ»ή“ΚΒΡœ¥ΤχΤΩΘ§ΖΔœ÷ΝΫ’ΏΖ÷±π‘ω÷Ί2.7gΚΆ6.6gΘ° | Θ®2Θ©AΒΡΖ÷Ή” ΫΈΣ C3H6O3 C3H6O3 |
| Θ®3Θ©Νμ»ΓA 4.5gΘ§ΗζΉψΝΩΒΡNaHCO3ΖέΡ©Ζ¥”ΠΘ§…ζ≥…1.12L CO2Θ§»τ”κΉψΝΩΫπ τΡΤΖ¥”Π‘ρ…ζ≥…1.12LH2Θ®ΤχΧεΧεΜΐΨυ‘Ύ±ξΉΦΉ¥Ωωœ¬≤βΕ®Θ©Θ° | Θ®3Θ©”ΟΫαΙΙΦρ Ϋ±μ ΨA÷–Κ§”–ΒΡΙΌΡήΆ≈ΘΚ -OH -OH ΓΔ-COOH -COOH Θ° |
Θ®4Θ©AΒΡΚΥ¥≈Ι≤’ώ«βΤΉ»γΆΦΘΚ |
Θ®4Θ©AΒΡΫαΙΙΦρ ΫΈΣΘΚ   |
 Θ®1Θ©ΦΉΈο÷ ÷ΜΚ§”–ΧΦΓΔ«βΝΫ÷÷‘ΣΥΊΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬ΈΣΤχΧ§Θ§”–ΜζΈοΦΉΒΡ≤ζΝΩΩ…“‘”Οά¥ΚβΝΩ“ΜΗωΙζΦ“ΒΡ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΘ°ΙΛ“Β…œΩ…“‘”Ο±ϊΈο÷ ά¥…ζ≤ζΦΉΈο÷ Θ§Ζ¥”Π Ϋ±μ ΨΘΚ
Θ®1Θ©ΦΉΈο÷ ÷ΜΚ§”–ΧΦΓΔ«βΝΫ÷÷‘ΣΥΊΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬ΈΣΤχΧ§Θ§”–ΜζΈοΦΉΒΡ≤ζΝΩΩ…“‘”Οά¥ΚβΝΩ“ΜΗωΙζΦ“ΒΡ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΘ°ΙΛ“Β…œΩ…“‘”Ο±ϊΈο÷ ά¥…ζ≤ζΦΉΈο÷ Θ§Ζ¥”Π Ϋ±μ ΨΘΚ| 500Γφ |
| CuΜρAg |
| Γς |
| CuΜρAg |
| Γς |
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com