
题目列表(包括答案和解析)

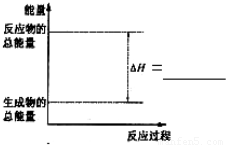
 Si(s)+4HCl(g)?该反应的反应热ΔH=
Si(s)+4HCl(g)?该反应的反应热ΔH=
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C | O=O |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 | 498 |
 Si(s)+4HCl(g),该反应的反应热△H=______
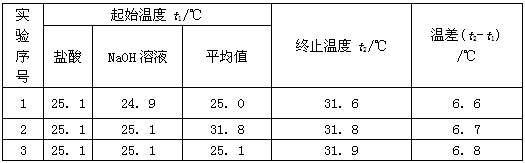
Si(s)+4HCl(g),该反应的反应热△H=______| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1) /℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 31.8 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
 本题由两部分组成
本题由两部分组成| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C | O=O |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 | 498 |
| ||
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1) /℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 31.8 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一。重庆一中某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究。
I. 甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,跟随父母来到重庆后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋。
②酿造醋国家标准为醋酸含量必须大于3.50 g/100mL,而配制醋国家标准仅为1.50 g~3.50g/100mL。
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助张同学计算从超市购买的食醋中醋酸含量为_______g/100mL,属于____________醋(填“酿造”或“配制”)。(提示:醋酸摩尔质量为60g/mol)
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_______________________________。
II. 下图是重庆一中化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配100mL1mol/L的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有 ;
(2)经计算,配制100mL1mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为 mL(保留小数点后一位);
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol/L,引起误差的原因可能是 。
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.转移溶液后,未洗涤烧杯和玻璃棒 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 |
作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一。重庆一中某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究。
I. 甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,跟随父母来到重庆后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋。
②酿造醋国家标准为醋酸含量必须大于3.50 g/100mL,而配制醋国家标准仅为1.50 g~3.50g/100mL。
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助张同学计算从超市购买的食醋中醋酸含量为_______g/100mL,属于____________醋(填“酿造”或“配制”)。(提示:醋酸摩尔质量为60g/mol)
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_______________________________。
II. 下图是重庆一中化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配100mL1mol/L的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:

(1)配制稀盐酸时,还缺少的仪器有 ;
(2)经计算,配制100mL1mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为 mL(保留小数点后一位);
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol/L,引起误差的原因可能是 。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
III. 丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣。
(1)他利用买来的鸡蛋的蛋清配制成溶液,用激光笔照射溶液,发现一条光束穿过鸡蛋清溶液,此现象称为____________________。
(2)他将乙同学配制好的盐酸溶液加入到鸡蛋清溶液中,发现出现絮状沉淀,此现象称为_________。
IV. 丁同学试图测定CO2的相对分子质量。
①利用丙同学用完后剩下的鸡蛋壳和乙同学配制好的稀盐酸溶液制备CO2;
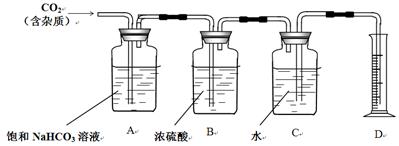
②查询相关书籍后,设计了如下装置:
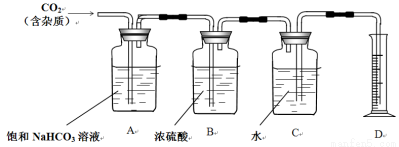
(1)B装置在此处____必要(填写“有”、“无”)请简述原因_________________________________。
(2)A装置中的饱和NaHCO3溶液可以吸收______________。
(3)实验前测得C装置(含水)重量为50.00g,实验完毕后C装置(含水)重量为40.02g,D中量筒读数为10.0 mL,已知H2密度为0.09g/L(以上数据均已折合为标况下数值),请根据以上数据,计算CO2的相对分子质量为____________(保留小数点后一位)。
一、单项选择题
1.D 2.C 3.B 4.C 5.D 6.C 7.A 8.B
二、不定项选择题
9.D 10.BC 11.D 12.AC 13.CD 14.A
三、非选择题(本题包括6小题,共60分)
15.(12分)
(1)500mL容量瓶 (1分)、玻璃棒(1分) 淀粉溶液 (1分)
(2)碱式(2分) 滴入最后一滴硫代硫酸钠溶液,溶液蓝色褪去,且半分钟内不恢复。(2分)(3)为保证I-全部转化为I2,所加氧化剂应稍过量。如果选用新制氯水或KMnO4作氧化剂,则过量的这些氧化剂在滴定时会氧化硫代硫酸钠而导致测定结果偏大。(2分)
(4)0.06410% (3分)
16.(8分)
----化学.files/image034.gif) (1)
(1分) CO(NH2)2 (1分)
(1)
(1分) CO(NH2)2 (1分)
(2) N2+Al2O3+----化学.files/image035.gif)
----化学.files/image036.gif) 3CO+2AlN (2分)
3CO+2AlN (2分)
(3) AlN+OH-+H2O =AlO----化学.files/image038.gif) +NH3↑ (2分)
+NH3↑ (2分)
(4) ④⑦ (2分)
17.(8分)
(1)温度较低(2分)
(2)AC(2分)
(3)2Fe3+ + 3ClO- + 10 OH- = 2FeO4-+ 3Cl-+ 5H2O (2分)
(4)B、D(2分)
18.(10分)
(1)CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g)
△H=一867 kJ?mol一1 (2分)
(2) Na2S+2H2O----化学.files/image040.gif) S↓+H2↑+2NaOH (2分) 或S2-+2H2O
S↓+H2↑+2NaOH (2分) 或S2-+2H2O----化学.files/image040.gif) S↓+H2↑+2OH-
S↓+H2↑+2OH-
(3)Ksp(HgS)<Ksp(FeS) (2分) 因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附悬浮杂质而净化水(2分)
(4)尿素法成本低,节约能源。(2分)
----化学.files/image041.gif) 19.(12分)
19.(12分)
(1) (2分)
(2) 3种 (2分)
(3) 6 (2分)
(4)A: ----化学.files/image043.jpg) (2分)
② 过氧化物、HBr(1分)
(2分)
② 过氧化物、HBr(1分)
----化学.files/image045.jpg) |
B: (2分) ④ 浓硫酸(1分)
20.(10分)
(1)不能 (1分) BaCO3会与胃酸反应产生Ba2+使人中毒 (2分) 或说由于存在溶解平衡:BaCO3(s) ----化学.files/image047.gif) Ba2+(aq)+CO32-(aq),服下BaCO3后,胃酸可与CO32-反应生成CO2和水,CO32-浓度降低,BaCO3的沉淀溶解平衡向右移动,Ba2+浓度增大引起人体中毒。
Ba2+(aq)+CO32-(aq),服下BaCO3后,胃酸可与CO32-反应生成CO2和水,CO32-浓度降低,BaCO3的沉淀溶解平衡向右移动,Ba2+浓度增大引起人体中毒。
(2)BaSO4(s)----化学.files/image048.gif) Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)
C(Ba2+)=1.1×10-10/0.36 =3.1×10-10 < 2×10-3mol?L-1
可以有效除去Ba2+ (3分)
(3)Ba2+ ~ BaCrO4 ~----化学.files/image050.gif) Cr2O72-~
Cr2O72-~----化学.files/image052.gif) I2~ 3S2O32-
I2~ 3S2O32-
1mol 3mol
36.00×0.100×10-3mol
c(Ba2+)----化学.files/image054.gif) mol?L-1
(4分)
mol?L-1
(4分)
四、选做题(本题包括1小题,共12分)
21.(12分)
(1)1s22s22p63s23p63d104s24p1 (2分)
(2)ACD (2分)
(3)非极性分子(2分) 三角锥 (2分) sp2 (2分)
(4)NH3分子间能形成氢键,而AsH3分子间不能形成氢键 (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com