
题目列表(包括答案和解析)
(18分)[探究实验一] 某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系):
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A. 浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色。 |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体。 |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:探究同周期主族元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液。仪器:① ,② ,③ ,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 |
|
|
| 2 |
|
|
| 3 |
|
|
| 4 |
|
|
| 5 |
|
|
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的强弱,请你设计实验(实验用品自选,不要求写化学方程式):
;
(5)实验结论: ;
[探究实验二] 一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
| 实验 序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式/ | 催化效果/g·g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 |
| 100 | 振动球磨 |
|
(注:催化效果用单位时间内每克催化剂得到产品的质量来表示)
(6)表中![]() = ;
= ;
(7)从实验1、2可以得出的结论是: ;
(8)设计实验2、3的目的是: 。
(18分)[探究实验一] 某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系):
|
实验步骤 |
实验现象 |
|
1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
A. 浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色。 |
|
2.向新制得的Na2S溶液中滴加少量新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
3.将一小块钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体。 |
|
4.将镁条投入稀盐酸中 |
D.反应不十分剧烈,产生无色气体 |
|
5.将铝条投入稀盐酸中 |
E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:探究同周期主族元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液。仪器:① ,② ,③ ,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
|
实验内容 |
实验现象 |
离子方程式 |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
|
5 |
|
|
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的强弱,请你设计实验(实验用品自选,不要求写化学方程式):
;
(5)实验结论: ;
[探究实验二] 一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
|
实验 序号 |
氯化镁固体中氯元素含量/% |
温度/℃ |
粉碎方式/ |
催化效果/g·g-1 |
|
1 |
70.97 |
20 |
滚动球磨 |
3.9×104 |
|
2 |
74.45 |
20 |
滚动球磨 |
5.0×104 |
|
3 |
74.45 |
20 |
振动球磨 |
5.9×104 |
|
4 |
|
100 |
振动球磨 |
|
(注:催化效果用单位时间内每克催化剂得到产品的质量来表示)
(6)表中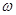 =
;
=
;
(7)从实验1、2可以得出的结论是: ;
(8)设计实验2、3的目的是: 。
|
元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
电负性 |
1.61 |
2.04 |
1.57 |
2.55 |
3.16 |
3.98 |
0.98 |
|
元 素 |
Mg |
N |
Na |
O |
P |
S |
Si |
|
电负性 |
1.31 |
3.04 |
0.93 |
3.44 |
2.19 |
2.58 |
1.90 |
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性的变化规律是:_______________________________________________________________________________。
(2)预测Br与Ⅰ元素电负性的大小关系________________,电负性最小的元素在周期表中的位置是:___________________________________(放射性元素除外)。
(3)习惯上把SrI2作为离子化合物,把BaS作为共价化合物。(电负性Sr=0.95;I=2.66;Ba=0.89;S=2.58)我们把两成键原子的电负性差值用DX表示,请找出用DX来判断离子键或共价键的数值范围:即当DX________时一般为离子键,当DX________时一般为共价键。试判断AlBr3中化学键的类型是________。
已知元素的电负性和原子半径等内容一样,也是元素的一种基本性质,下面给出14种元素的电负性:
|
元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
电负性 |
1.61 |
2.04 |
1.57 |
2.55 |
3.16 |
3.98 |
0.98 |
|
元 素 |
Mg |
N |
Na |
O |
P |
S |
Si |
|
电负性 |
1.31 |
3.04 |
0.93 |
3.44 |
2.19 |
2.58 |
1.90 |
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性的变化规律是:_______________________________________________________________________________。
(2)预测Br与Ⅰ元素电负性的大小关系________________,电负性最小的元素在周期表中的位置是:___________________________________(放射性元素除外)。
(3)习惯上把SrI2作为离子化合物,把BaS作为共价化合物。(电负性Sr=0.95;I=2.66;Ba=0.89;S=2.58)我们把两成键原子的电负性差值用DX表示,请找出用DX来判断离子键或共价键的数值范围:即当DX________时一般为离子键,当DX________时一般为共价键。试判断AlBr3中化学键的类型是________。
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出12种元素的X的数值:
|
元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
X的数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
|
元素 |
Mg |
Na |
O |
P |
S |
Si |
N |
|
X的数值 |
|
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
|
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系______________________________。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某有机物结构简式为: ,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
(5) 预测元素周期表中,X值最小的元素位置________(放射性元素除外)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com