
题目列表(包括答案和解析)
(10镇江24).(4分)某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:

(1)操作①、②、③依次为下图中的(填字母) ▲ 。

(2)若NaCl的产率偏低(  ),则可能的原因是(填字母) ▲ 。
),则可能的原因是(填字母) ▲ 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5%NaCl溶液50.0g,需称取NaCl ▲ g,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、 ▲ 。
(10镇江30).(14分)将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对蓝色固体的成分进行了如下探究。请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由: ▲ (用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈 ▲ (填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经 ▲ 、洗涤、低温烘干得蓝色固体。
(2)判断固体已洗净的方法及现象 ▲ 。
Ⅱ.用下图所示装置,定性探究固体的成分。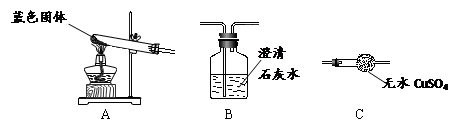
(3)若用装置A、B组合进行实验,B中无现象,则猜想 ▲ 正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想 ▲ 正确;
(5)小组同学将装置按 A、 ▲ 、 ▲ (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为 ▲ ,C中的现象为 ▲ 。
结论:固体为Cu(OH)2和CuCO3的混合物。
Ⅲ.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体
的组成为aCu(OH)2?bCuCO3。小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图,请根据图示回答下列问题: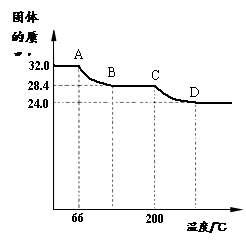
(6)写出A B、C D段发生反应的化学方程式:
AB段: ▲ ;
CD段: ▲ ;
(7)通过计算可得: a:b= 。
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式: ▲ 。
(10镇江27).(6分)有一实验事实:铁粉与硫酸铜溶液反应,不但有铜生成,而且有较多的气体产生。为确定气体的成分,进行下列实验探究。
(一)探究:从物质组成元素角度分析,气体可能是SO2、O2、H2中的一种或几种。
(二)实验:
(1)甲同学为确定是否含有SO2,他将气体通入酸性高锰酸钾溶液中,溶液颜色未发生变化,则该气体中 ▲ SO2(填“有”或“无”)。
(2)乙同学认为只有O2,则可用是 ▲ 来检验。实验证明乙同学的观点不正确
(3)丙同学为判断是否含有O2,同时确定气体成分,通过查阅资料得知:
O2+4KI+4HCl=2I2+4KCl+2H2O,I2为碘单质。于是他设计了如下的实验装置:
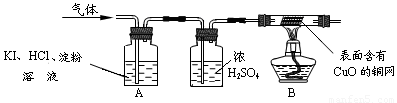
(三)实验现象与结论:A中观察到 ▲ ,证明无O2;
B中观察到 ▲ ,证明该气体是H2。
(四)实验反思:
(4)大家认为丙同学在加热之前,应对气体先 ▲ 以确保安全。
(5)由上述实验可知,硫酸铜溶液显 ▲ 性(填“酸”或“碱”)。
(10镇江30).(14分)将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对蓝色固体的成分进行了如下探究。请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由: ▲ (用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈 ▲ (填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经 ▲ 、洗涤、低温烘干得蓝色固体。
(2)判断固体已洗净的方法及现象 ▲ 。
Ⅱ.用下图所示装置,定性探究固体的成分。
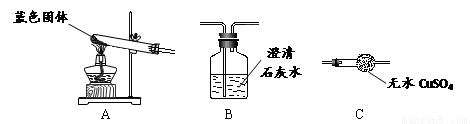
(3)若用装置A、B组合进行实验,B中无现象,则猜想 ▲ 正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想 ▲ 正确;
(5)小组同学将装置按 A、 ▲ 、 ▲ (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为 ▲ ,C中的现象为 ▲ 。
结论:固体为Cu(OH)2和CuCO3的混合物。
Ⅲ.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体
的组成为aCu(OH)2•bCuCO3。小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图,请根据图示回答下列问题:
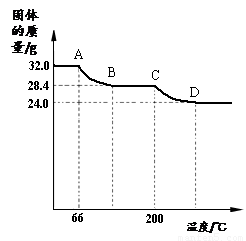
(6)写出A B、C D段发生反应的化学方程式:
AB段: ▲ ;
CD段: ▲ ;
(7)通过计算可得: a:b= 。
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式: ▲ 。
(10镇江24).(4分)某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
(1)操作①、②、③依次为下图中的(填字母) ▲ 。
(2)若NaCl的产率偏低( ),则可能的原因是(填字母) ▲ 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5%NaCl溶液50.0g,需称取NaCl ▲ g,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com