
题目列表(包括答案和解析)
卤族元素的单质和化合物很多,请利用所学物质结构与性质的相关知识回答下列问题:
(1)卤族元素位于周期表的 ????????? 区;氟原子的电子排布图为?????? 溴原子的价电子排布式为????? .
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是??????????
(3)已知高碘酸有两种形式,化学式分别为H5IO6 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大。这是由于溶液中发生下列反应 I-+ I2 =I3-与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 ??? 式发生。
A.CsICl2=CsCl+ICl?????? B.CsICl2 =CsI +Cl2
(5)ClO2-的空间构型为?????? 型,中心氯原子的杂化轨道类型为???????? ,写出一个ClO2-的等电子体 ???????????? 。
(6)如图为碘晶体晶胞结构。有关说法中正确的是???? 。

A.碘分子的排列有2种不同的取向
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3 .NA为阿伏加德罗常数,相邻的两个Ca2+核间距为a cm,则CaF2的摩尔质量可以表示为?????? 。
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于周期表的_______区;溴的价电子排布式为____________________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是________________。
(3)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是_________。
| 氟 | 氯 | 溴 | 碘 | 铍 |
第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
(4)已知高碘酸有两种形式,化学式分别为H5IO6( )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
(5)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应I-+I2=I3-。与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列_____式发生。
A.CsICl2=CsCl+ICl??????? B.CsICl2=CsI+Cl2
(6)已知ClO2-为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为___________,写出一个ClO2-的等电子体__________。
(7)已知CaF2晶体(见图)的密度为ρ g·cm-3,NA为阿伏加德罗常数,最近相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为___________。

(10分)羟基亚乙基二磷酸(HEDPA,结构式如右图,可简写为H4L)可在较宽的pH范围内与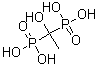 金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250℃以上样品失重25.80%。脱水结束后对残余物之进行元素分析。配合物A的元素含量为:Mn(15.74%);C(6.88%);H(4.62%);O(55.01%);P(17.77%)。 问:
金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250℃以上样品失重25.80%。脱水结束后对残余物之进行元素分析。配合物A的元素含量为:Mn(15.74%);C(6.88%);H(4.62%);O(55.01%);P(17.77%)。 问:
4-1 根据元素分析数据,推证配合物A的分子式为_______________________________
4-2 画出该配合物的结构示意图,并在图上注明HEDPA中哪些原子可为配位原子?(用*表示)
4-3 实验测得配合物A的磁矩为6.12 μ0,配合物未成对电子数为________,中心原子的杂化轨道类型是______________________________________________
4-4 如何将合成A的条件作修改,可得到多核配合物?并写出2种该多核配合物的分子式。
___________________________________________________________________________
___________________________________________________________________________
4-5 已知配合物[Mn(H2O)6]2+的d-d跃迁在400 nm -550 nm范围内有弱的吸收,配合物呈肉粉色;在水溶液中形成配合物Ⅱ后,中心离子的晶体场分裂能将发生怎样的变化?观察配合物的颜色明显加深,为什么?
___________________________________________________________________________
___________________________________________________________________________
现有部分短周期主族元素的有关信息,如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
核外有5种不同能量的电子,其中有2个未成对电子 |
|
X |
最高化合价为+7价 |
|
Y |
短周期主族元素原子中半径最大 |
|
Z |
地壳中含量最多的金属 |
(1)T的一种单质相对分子质量为256,能溶于CS2,该单质的分子式为____________(用元素符号表示);指出T单质的一种用途_____________________________。
⑵写出Z氢氧化物的电离方程式:;下列酸中不能溶解Z单质的是。
a.浓硝酸 b.热浓硫酸 c.浓盐酸 d.稀硝酸
⑶可用于扑灭Y单质燃烧引起的火灾的物质是___________。
a.二氧化碳 b.水 c.沙土 d.干粉(主要成分为NaHCO3)
⑷.元素X元素T相比,非金属性较强的是__________(用元素符号表示)。下列表述中能证明这一事实的是____________。
a.在溶液中T的单质能置换出X的单质
b.X的气态氢化物比T的气态氢化物更稳定
c.T的无氧酸钠盐溶液pH>7,而X的+7价含氧酸钠盐溶液pH=7
现有部分短周期主族元素的有关信息,如下表:
| 元素编号 | 元素性质或原子结构 |
| T | 核外有5种不同能量的电子,其中有2个未成对电子 |
| X | 最高化合价为+7价 |
| Y | 短周期主族元素原子中半径最大 |
| Z | 地壳中含量最多的金属 |
(1)T的一种单质相对分子质量为256,能溶于CS2,该单质的分子式为____________(用元素符号表示);指出T单质的一种用途_____________________________。
⑵写出Z氢氧化物的电离方程式:;下列酸中不能溶解Z单质的是。
a.浓硝酸 b.热浓硫酸 c.浓盐酸 d.稀硝酸
⑶可用于扑灭Y单质燃烧引起的火灾的物质是___________。
a.二氧化碳 b.水 c.沙土 d.干粉(主要成分为NaHCO3)
⑷.元素X元素T相比,非金属性较强的是__________(用元素符号表示)。下列表述中能证明这一事实的是____________。
a.在溶液中T的单质能置换出X的单质
b.X的气态氢化物比T的气态氢化物更稳定
c.T的无氧酸钠盐溶液pH>7,而X的+7价含氧酸钠盐溶液pH=7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com