
题目列表(包括答案和解析)
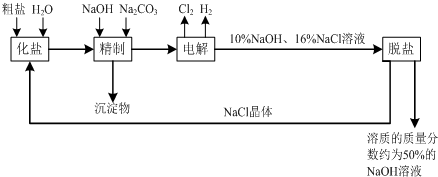


工业上主要采用电解饱和食盐水的方法来制取Cl2、H2、NaOH。请回答下列问题:
(1)在电解过程中,所发生反应的离子反应方程式为: ;
(2)电解之前食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:a、Na2CO3溶液 b、Ba(OH)2溶液 c、稀盐酸。其中合理的加入顺序为 (填写序号) ;
(3)如果在容积为10L的电解池内,一段时间后共收集到11.2L(标准状况)气体。这时溶液中NaOH的物质的量浓度为 (设电解时溶液的体积不变)。
工业上主要采用电解饱和食盐水的方法来制取Cl2、H2、NaOH。请回答下列问题:
(1)在电解过程中,所发生反应的离子反应方程式为: ;
(2)电解之前食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:a、Na2CO3溶液 b、Ba(OH)2溶液 c、稀盐酸。其中合理的加入顺序为 (填写序号) ;
(3)如果在容积为10L的电解池内,一段时间后共收集到11.2L(标准状况)气体。这时溶液中NaOH的物质的量浓度为 (设电解时溶液的体积不变)。

| ||
| ||
 则以下叙述正确的是
则以下叙述正确的是湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com