(2009?广州模拟)某探究小组用KMnO
4酸性溶液与H
2C
2O
4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
(1)该反应的离子方程式为(提示:H
2C
2O
4的一级电离常数为5.4×10
-2)
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
.
(2)实验条件作如下限定:所用KMnO
4酸性溶液的浓度可选择0.01mol?L
-1、0.001mol?L
-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO
4酸性溶液的用量均为4mL、H
2C
2O
4溶液(0.1mol?L
-1)的用量均为2mL.如果要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成
4
4
个实验进行对比即可得出结论.
(3)在其它条件相同的情况下,某同学改变KMnO
4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液
的浓度/mol?L-1 |
溶液褪色所需时间 t/min |
| 第1次 |
第2次 |
第3次 |
| 0.01 |
14 |
13 |
11 |
| 0.001 |
6 |
7 |
7 |
①计算用0.001mol?L
-1 KMnO
4酸性溶液进行实验时KMnO
4的平均反应速率(忽略混合前后溶液的体积变化,写出计算过程).
②若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?
不可行
不可行
.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:
取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应.
取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应.
.



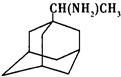 中新网2009年5月21日电:据法新社报道,世界卫生组织宣布全球感染甲型H1N1流感患者已升至11034人.根据所有的资料显示,“达菲”是国际上公认的治疗流感的药物之一.广东省中医院呼吸内科主任林琳教授解释,目前我们常用的抗病毒药有两大类,一个是金刚烷胺类药物,另一个是神经氨酸酶抑制剂类药物.据现在研究的情况,甲型H1N1流感病毒对金刚烷胺类药物不敏感,而对神经氨酸酶抑制剂类药物如达菲还是敏感的.
中新网2009年5月21日电:据法新社报道,世界卫生组织宣布全球感染甲型H1N1流感患者已升至11034人.根据所有的资料显示,“达菲”是国际上公认的治疗流感的药物之一.广东省中医院呼吸内科主任林琳教授解释,目前我们常用的抗病毒药有两大类,一个是金刚烷胺类药物,另一个是神经氨酸酶抑制剂类药物.据现在研究的情况,甲型H1N1流感病毒对金刚烷胺类药物不敏感,而对神经氨酸酶抑制剂类药物如达菲还是敏感的.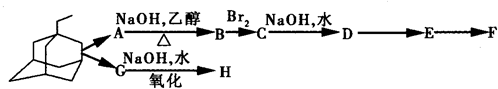
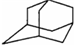 )
)

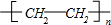
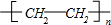
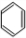 +Br2
+Br2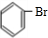 +HBr
+HBr +Br2
+Br2 +HBr
+HBr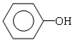 )和丙酮(CH3COCH3).生产流程如下:
)和丙酮(CH3COCH3).生产流程如下: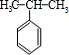

 +O2
+O2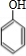 +
+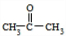
 +O2
+O2 +
+