ΔώΘ°“Μ―θΜ·ΧΦ «“Μ÷÷”ΟΆΨœύΒ±ΙψΖΚΒΡΜ·ΙΛΜυ¥Γ‘≠ΝœΘ°
Θ®1Θ©άϊ”Οœ¬Ν–Ζ¥”ΠΩ…“‘ΫΪ¥÷ΡχΉΣΜ·ΈΣ¥ΩΕ»¥ο99.9%ΒΡΗΏ¥ΩΡχΘ°
NiΘ®sΘ©+4COΘ®gΘ©

NiΘ®COΘ©
4Θ®gΘ© ΗΟΖ¥”ΠΒΡΓςH
ΘΦ
ΘΦ
0 Θ®―ΓΧνΓΑΘΨΓ±ΜρΓΑ=Γ±ΜρΓΑΘΦΓ±Θ©Θ°
Θ®2Θ©‘ΎΗΏΈ¬œ¬“Μ―θΜ·ΧΦΩ…ΫΪΕΰ―θΜ·ΝρΜΙ‘≠ΈΣΒΞ÷ ΝρΘ°“―÷ΣΘΚ
CΘ®sΘ©+O
2Θ®gΘ©=CO
2Θ®gΘ©ΓςH
1=-393.5kJ?mol
-1CO
2Θ®gΘ©+CΘ®sΘ©=2COΘ®gΘ©ΓςH
2=+172.5kJ?mol
-1SΘ®sΘ©+O
2Θ®gΘ©=SO
2Θ®gΘ©ΓςH
3=-296.0kJ?mol
-1«κ–¥≥ωCO≥ΐSO
2ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ
2COΘ®gΘ©+SO2Θ®gΘ©=SΘ®sΘ©+2CO2Θ®gΘ©ΓςH3=-270kJ?mol-1
2COΘ®gΘ©+SO2Θ®gΘ©=SΘ®sΘ©+2CO2Θ®gΘ©ΓςH3=-270kJ?mol-1
Θ°
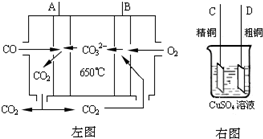
Θ®3Θ©»γΆΦ÷–ΉσΆΦ «“ΜΧΦΥα―Έ»ΦΝœΒγ≥ΊΘ§Υϋ“‘COΈΣ»ΦΝœΘ§“ΜΕ®±»άΐLi
2CO
3ΚΆNa
2CO
3ΒΆ»έΜλΚœΈοΈΣΒγΫβ÷ Θ§”“ΆΦ «¥÷Ά≠ΨΪΝΕΒΡΉΑ÷ΟΆΦΘ§œ÷”Ο»ΦΝœΒγ≥ΊΈΣΒγ‘¥Ϋχ––¥÷Ά≠ΒΡΨΪΝΕ Β―ιΘ°ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ–¥≥ωAΦΪΖΔ…ζΒΡΒγΦΪΖ¥”Π Ϋ
CO-2e-+CO32-=2CO2
CO-2e-+CO32-=2CO2
Θ°
ΔΎ“Σ”Ο»ΦΝœΒγ≥ΊΈΣΒγ‘¥Ϋχ––¥÷Ά≠ΒΡΨΪΝΕ Β―ιΘ§‘ρBΦΪ”ΠΗΟ”κ
D
D
ΦΪ Θ®ΧνΘΚΓΑCΓ±ΜρΓΑDΓ±Θ©œύΝ§Θ°
ΔέΒ±œϊΚΡ2.24LΘ®±ξΩωœ¬Θ©CO ±Θ§¥÷Ά≠ΒγΦΪάμ¬έ…œΦθ…ΌΆ≠ΒΡ÷ ΝΩ
–Γ”Ύ
–Γ”Ύ
Θ®ΧνΘΚΓΑ¥σ”ΎΓ±ΓΔΓΑΒ»”ΎΓ±ΜρΓΑ–Γ”ΎΓ±Θ©6.4ΩΥΘ°
ΔρΘ°Θ®1Θ©“―÷ΣNa
2CrO
4»ή“ΚΥαΜ· ±ΖΔ…ζΒΡΖ¥”ΠΈΣΘΚ2CrO
42-+2H
+?Cr
2O
72-+H
2OΘ§»τ1LΥαΜ·ΚσΥυΒΟ»ή“Κ÷–Ηθ‘ΣΥΊΒΡΉήΈο÷ ΒΡΝΩΈΣ0.55molΘ§CrO
42-”–
ΉΣΜ·ΈΣCr
2O
72-Θ°”÷÷ΣΘΚ≥ΘΈ¬ ±ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK=10
14Θ°…œ ωΥαΜ·ΚσΥυΒΟ»ή“ΚΒΡpH=
6
6
Θ°
Θ®2Θ©ΗυΨί”–ΙΊΙζΦ“±ξΉΦΘ§Κ§CrO
42-ΒΡΖœΥ°“ΣΨ≠Μ·―ߥΠάμΘ§ ΙΤδ≈®Ε»ΫΒ÷Ν5.0ΓΝ10
-7mol?L
-1“‘œ¬≤≈Ρή≈≈Ζ≈Θ°Κ§CrO
42-ΒΡΖœΥ°¥ΠάμΆ®≥Θ”–“‘œ¬ΝΫ÷÷ΖΫΖ®Θ°
ΔΌ≥ΝΒμΖ®ΘΚΦ”»κΩ…»ή–‘±Β―Έ…ζ≥…BaCrO
4≥ΝΒμ[K
spΘ®BaCrO
4Θ©=1.2ΓΝ10
-10]Θ§‘ΌΦ”»κΩ…»ή–‘ΝρΥα―Έ¥ΠάμΕύ”ύΒΡBa
2+Θ°Φ”»κΩ…»ή–‘±Β―ΈΚσΒΡΖœΥ°÷–Ba
2+ΒΡ≈®Ε»”Π≤Μ–Γ”Ύ
2.4ΓΝ10-4
2.4ΓΝ10-4
mol?L
-1Θ§»ΜΚσ‘ΌΫχ––Κσ–χ¥ΠάμΖΫΡή¥οΒΫΙζΦ“≈≈Ζ≈±ξΉΦΘ°
ΔΎΜΙ‘≠Ζ®ΘΚCrO
42-Cr
3+CrΘ®OHΘ©
3Θ°”ΟΗΟΖΫΖ®¥Πάμ10m
3 CrO
42-ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ1.0ΓΝ10
-3 mol?L
-1ΒΡΖœΥ°Θ§÷Ν…Ό–η“Σ¬ΧΖ·Θ®FeSO
4?7H
2OΘ§œύΕ‘Ζ÷Ή”÷ ΝΩΈΣ278Θ©
8.34
8.34
KgΘ®±ΘΝτΝΫΈΜ–Γ ΐΘ©Θ°

 Θ®2010?…«ΆΖ“ΜΡΘΘ©Ηθ «»ΥΧε±Ί–η‘ΣΥΊΘ§»γΚ§ΝΩ≤ΜΉψΜα”ΑœλΧ«άύΚΆ÷§άύΒΡ¥ζ–ΜΘ§ΙΐΗΏ‘ρΜα“ΐΤπΦ±–‘÷–ΕΨΘ°”–ΙΊΚ§ΗθΜ·ΚœΈοΒΡœύΜΞΉΣΜ·ΙΊœΒ»γœ¬
Θ®2010?…«ΆΖ“ΜΡΘΘ©Ηθ «»ΥΧε±Ί–η‘ΣΥΊΘ§»γΚ§ΝΩ≤ΜΉψΜα”ΑœλΧ«άύΚΆ÷§άύΒΡ¥ζ–ΜΘ§ΙΐΗΏ‘ρΜα“ΐΤπΦ±–‘÷–ΕΨΘ°”–ΙΊΚ§ΗθΜ·ΚœΈοΒΡœύΜΞΉΣΜ·ΙΊœΒ»γœ¬ Cr2O72-+H2O
Cr2O72-+H2O Cr2O72-+H2O
Cr2O72-+H2O NiΘ®COΘ©4Θ®gΘ© ΗΟΖ¥”ΠΒΡΓςH
NiΘ®COΘ©4Θ®gΘ© ΗΟΖ¥”ΠΒΡΓςH

 Cr2O72-+H2O
Cr2O72-+H2O Cr2O72-+H2O
Cr2O72-+H2O