
题目列表(包括答案和解析)

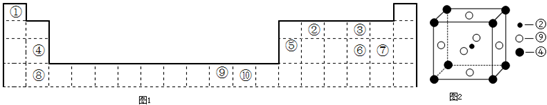
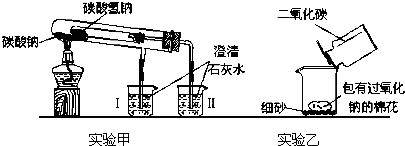

(20分)下图是两个实验装置(铁架台等辅助仪器略去未画)
回答下列问题:
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是 (填“Ⅰ”、“Ⅱ”)烧杯,该烧杯中发生反应的离子方程式是: ,通过实验甲可比较出Na2CO3、NaHCO3两种固体, 更稳定。
(2)实验乙用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花着火燃烧。写出Na2O2与CO2反应的化学方程式 ,棉花能着火燃烧说明该反应特点是 。
(3)取10.0g碳酸钠和碳酸氢钠的混合物充分进行加热,将生成的CO2气体通入足量澄清石灰水中完全吸收,测得生成沉淀4.0g。求(要求写出计算过程):
①生成的CO2气体体积(标准状况下)
②原混合物中碳酸钠的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com