
题目列表(包括答案和解析)

| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 变红 变红 |
褪色 褪色 |
褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | 还原性 还原性 |
氧化性 氧化性 |

| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | ______ |

| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 变红 变红 |
褪色 褪色 |
褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | 还原性 还原性 |
氧化性 |
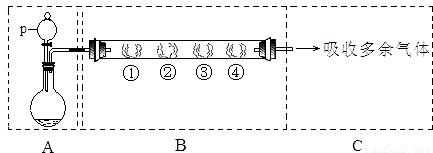
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
8.34 g FeSO4·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示.
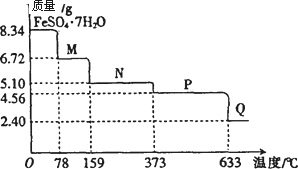
请回答下列问题:
(1)试确定78℃时固体物质M的化学式:________ .
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,写出该反应的化学方程式________ .
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响).
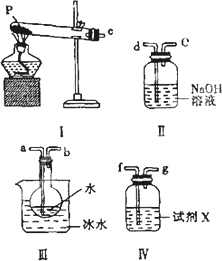
①试剂X的名称是________.
②按气流方向连接各仪器,用字母表示接口的连接顺序:c→________.
③充分反应后,利用装置Ⅲ中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重.第三步:继续烘干、冷却并称量直至连续两次称量的质量差不超过0.1 g为止.若最终得到沉淀的质量为Wg,则已分解的P的质量________(填计算式)________.
第Ⅰ卷(选择题 共45分)
选择题 (1~15题,每题3分,共45分)
题 号
1
2
3
4
5
6
7
8
选 项
B
A
D
D
B
A
D
C
题 号
9
10
11
12
13
14
15
选 项
D
A
B
C
B
C
B
第Ⅱ卷(非选择题 共55分)
说明:1.合理答案均可酌情给分,但不得超过原题分数。
2.若化学方程式2分,不写条件扣1分,不配平扣1分。不写可逆符号扣1分,不得
负分。若化学方程1分,不写条件或不配平不得分。
3.除标注外,其余每空1分,不出现0.5分。
16.(共6分)
(1)4FeS2+11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
(2)C
(3)A B(2分。多选、错选均不得分;选对一个且正确得1分)
(4)氨水 (NH4)2SO3+H2SO4  (NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
(NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
 17.(共7分)
17.(共7分)
(1)CH3CH2OH
CH2 CH2↑+ H2
O ①④⑤(多选、少选、错选均不
CH2↑+ H2
O ①④⑤(多选、少选、错选均不
得分)
 (2) 三角锥形 3Fe+8H++2NO
(2) 三角锥形 3Fe+8H++2NO
 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
(3)Al3+
+3AlO +6H2O
+6H2O  4Al(OH)
3↓ 2Al+2H2O+2OH
4Al(OH)
3↓ 2Al+2H2O+2OH
 2AlO
2AlO +3H2↑
+3H2↑
18.(共9分)
(1)2H2O2 2H2O+ O2↑
2H2O+ O2↑
(2)①③ (2分。多选、错选均不得分;选对一个且正确得1分)
(3)c(S2-)= [c(Na+)+c(H+)
[c(Na+)+c(H+) c (HS-)
c (HS-) c(OH
c(OH )]
)]
或c(S2-)= c (Na+)
c (Na+) c(HS
c(HS )
) c (H2S) (2分)
c (H2S) (2分)
(4)
19.(共8分)
(1)Fe3+、Al3+、Mg2+、H+(多写、少写、写错均不得分)
(2)SiO2+ Si+2CO↑
Si+2CO↑
AlO +CO2+ 2H2 O
+CO2+ 2H2 O  Al(OH)3↓+HCO
Al(OH)3↓+HCO (2分)
(2分)
(3)c d(2分。多选,错选均不得分;选对一个且正确得1分)
(4)电解 防止Mg2+水解,并带走水分,(答出“防止Mg2+水解”即可给分)
20.(共11分)
Ⅰ.(1)分液漏斗
B中棉花位置
①
②
③
④
所蘸试剂
现象
变红
褪色
体现的性质
还原性
(2)I2+SO2+2H2O
 4H+ +SO
4H+ +SO +2I
+2I
Ⅱ.(1)浓H2SO4
(2)Cl2+2I
 I2+2Cl
I2+2Cl b
b
(3)先由紫色变红色,后褪色
(4)5Cl2
+I2+6H2O  10Cl
10Cl +2IO
+2IO +12H+(2分)
+12H+(2分)
21.(共9分)
 |
22.(共5分)
(1)0.01 mol/L?s
(2)③④
(3)75%,<,
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com