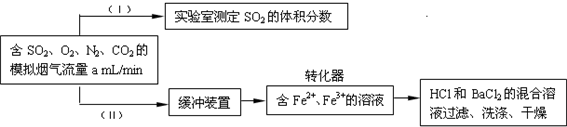
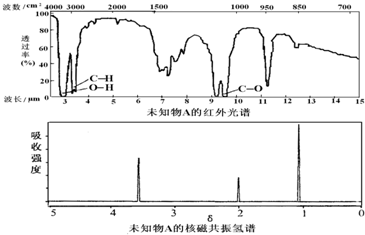
(2008?镇江二模)下列图1中B是一种常见的无色无味的液体.C是一种有磁性的化合物,E是一种无色无味的有毒气体.根据下列图1、图2,回答下列问题:

(1)写出C的化学式:
Fe3O4
Fe3O4
.
(2)E和N
2是等电子体,请写出可能E的电子式:
.
(3)在101kPa和150℃时,可逆反应E(g)+B(g)

F(g)+D(g)反应速率和时间的关系如图2所示,那么在t
1时速率发生改变的原因可能是(填选项字母)
B、C
B、C
.
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16g G和足量的A反应放出的热量为Q kJ(Q>0),写出这个反应的热化学方程式:
S(s)+Fe(s) =FeS(s);△H=-2Q kJ?mol-1
S(s)+Fe(s) =FeS(s);△H=-2Q kJ?mol-1
.
若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式:
C6H5OH
C6H5OH
;H的水溶液呈酸性,请用离子方程式表示呈酸性的原因:
Fe
3++3H
2O

Fe(OH)
3+3H
+Fe
3++3H
2O

Fe(OH)
3+3H
+.




 F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) Fe(OH)3+3H+
Fe(OH)3+3H+ Fe(OH)3+3H+
Fe(OH)3+3H+