
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
| ±àºÅ | »¯Ñ§·½³̀ʽ | ƽºâ³£Êư | ÎÂ¶È | |
| 979K | 1173K | |||
| ¢ñ | Fe£¨s£©+CO2?FeO£¨s£©+CO£¨g£© | K1 | 1.47 | 2.15 |
| ¢̣ | CO£¨g£©+H2O£¨g£©?CO2£¨g£©+H2£¨g£© | K2 | 1.62 | b |
| ¢ó | Fe£¨s£©+H2O£¨g£©? FeO£¨s£©+H2£¨g£© |
K3 | a | 1.68 |
| A¡¢a£¾b |
| B¡¢Ôö´óѹǿ£»Æ½ºâ×´̀¬II²»̉ƶ¯ |
| C¡¢Éư¸ßζÈƽºâ×´̀¬¢óỊ̈Ơư·´Ó¦·½Ị̈̉ƶ¯ |
| D¡¢·´Ó¦¢̣£¬¢ó¾ùΪ·ÅÈÈ·´Ó¦ |
| ±àºÅ | »¯Ñ§·½³̀ʽ | ƽºâ³£Êư | ÎÂ¶È | |
| 979K | 1173K | |||
| ¢ñ | Fe£¨s£©+CO2?FeO£¨s£©+CO£¨g£© | K1 | 1.47 | 2.15 |
| ¢̣ | CO£¨g£©+H2O£¨g£©?CO2£¨g£©+H2£¨g£© | K2 | 1.62 | b |
| ¢ó | Fe£¨s£©+H2O£¨g£©? FeO£¨s£©+H2£¨g£© |
K3 | a | 1.68 |
| A¡¢a£¾b |
| B¡¢Éư¸ßζÈƽºâ×´̀¬¢óỊ̈Ơư·´Ó¦·½Ị̈̉ƶ¯ |
| C¡¢Ôö´óѹǿ£»Æ½ºâ×´̀¬¢̣²»̉ƶ¯ |
| D¡¢·´Ó¦¢̣¡¢¢ó¾ùΪ·ÅÈÈ·´Ó¦ |
»¯Ñ§Æ½ºâ×´̀¬I¡¢II¡¢IIIµÄÏà¹ØÊư¾ƯÈçÏÂ±í£º
| ±àºÅ | »¯Ñ§·½³̀ʽ | ƽºâ³£Êư | ÎÂ¶È | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 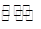 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 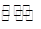 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)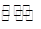 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
»¯Ñ§Æ½ºâ×´̀¬µÄÅжÏ̉À¾Ư£®
¢Ù________£»¢Ú________£®
»¯Ñ§Æ½ºâ×´̀¬I¡¢II¡¢¢óµÄÏà¹ØÊư¾ƯÈçÏÂ±í£º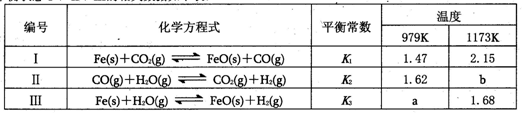
¸ù¾ỬÔÉÏĐÅÏ¢ÅĐ¶Ï£¬ÏÂÁĐ½áÂÛ´íÎóµÄÊÇ
| A£®a>b |
| B£®Éư¸ßζÈƽºâ×´̀¬¢óỊ̈Ơư·´Ó¦·½Ị̈̉ƶ¯ |
| C£®Ôö´óѹǿ£»Æ½ºâ×´̀¬II²»̉ƶ¯ |
| D£®·´Ó¦II¡¢¢ó¾ùΪ·ÅÈÈ·´Ó¦ |
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com