
äãá¢êÅÝÚ(¯■â´ÇÞ¯¡¤ë§ãö—)
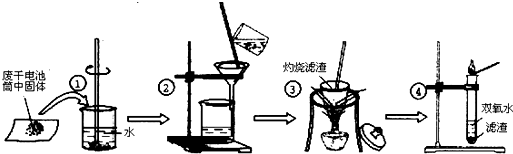

 Ș¡¤¥¨ñÇÆÎöˆFe-2e-´TFe2+È˜í»¥¨ñÇÆÎöˆCu2++2e-´TCu
Ș¡¤¥¨ñÇÆÎöˆFe-2e-´TFe2+È˜í»¥¨ñÇÆÎöˆCu2++2e-´TCu Ș¡¤¥¨ñÇÆÎöˆFe-2e-´TFe2+È˜í»¥¨ñÇÆÎöˆCu2++2e-´TCu
Ș¡¤¥¨ñÇÆÎöˆFe-2e-´TFe2+È˜í»¥¨ñÇÆÎöˆCu2++2e-´TCu| òçîÕý§øÒ | òçîÕüøüµ | òçîÕ§ÃôÜ¥¯âŠæÆñ§°äò§ |
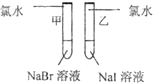 |
¥æ àÉؤÆèößè¨Ýðöˆ°àè¨ àÉؤÆèößè¨Ýðöˆ°àè¨ ØØ àÉؤÆèößè¨Ýðöˆ£óè¨ àÉؤÆèößè¨Ýðöˆ£óè¨ |
âŠæÆñ§°äò§ ¥æȤ 2Br-+Cl2´TBr2+2Cl- 2Br-+Cl2´TBr2+2Cl- ØØȤ 2I-+Cl2´T2Cl-+I2 2I-+Cl2´T2Cl-+I2 §ÃôÜȤôÝùÄçËøòçáî¾£₤ú¢ç§à¾çáù°Å·öˆCl2ȃBr2ȃI2 |
| òçîÕý§øÒ | òçîÕüøüµ | òçîÕØâƒï¤ë§ÃôÜ |
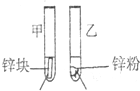 3mL1mol/L 3mL3mol/L îöùà îöùà ȴ§Þò¶øòê¢üÁë˜È˜îöùê¿»ê¢Èˋ |
ƒªÆÅó½äÍ躰èȘŢñÜüàü«òÏȘŢ¢Õ¤µü«òÏ | Ø·öˆØØòå¿ÉøÅçáñÇÆΡ■¢šÈ˜ùªØåñÇÆÎöÿé´Ñàå§ÇµÈ˜ñÇÆÎùìôò姢šÈÛ |

 Ñ₤È´äŸÀ¯ü·æµÀÝÀÂÀ¯ü·ÆØÀÝ£·À¯ý£ÀÝÈˋÈÛ
Ñ₤È´äŸÀ¯ü·æµÀÝÀÂÀ¯ü·ÆØÀÝ£·À¯ý£ÀÝÈˋÈÛ

¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com