
题目列表(包括答案和解析)

(1)X的化学式为__________________,O的结构简式为__________________。
(2)考虑到综合经济效益,工业生产M时,可采取的措施有__________________(填序号)。
a.使用催化剂 b.适当降低温度
c.选择合适的温度 d.适度增大压强
e.及时分离出产物 f.对原料进行循环利用
g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市
i.工厂地址可选择在盛产天然气的地区
(3)设备I的名称__________。工业生产中为了节约资源、降低成本和保护环境,常常对某些物质进行循环利用。上述转化关系中能达到该目的的是__________(填序号)。
(4)现有1 mol A参加反应,假设各步均完全反应,生成N的质量为
物质之间的转化关系如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,X的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见氮肥,且反应⑦中L与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素。
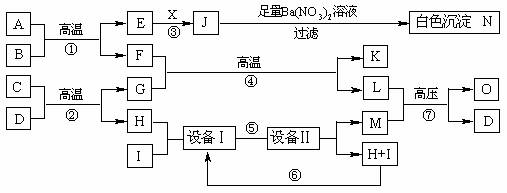
回答下列问题:
(1)X的化学式为___________,C+D的反应方程式为____ _______ ;
(2)写出反应⑦的化学方程式_____________________________________;
(3)现有1molA参加反应,假设各步反应均完全,生成N的质量为1165g,生成K的质量为224g,则反应①的化学方程式为_____________________。
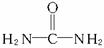
回答下列问题:
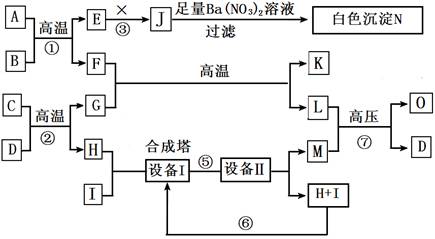
(1)X的化学式为_____________,O的结构简式为_________________。
(2)考虑到综合经济效益,工业生产M时,可采取的措施有____________(填序号)。
a.使用催化剂 b.适当降低温度 c.选择合适的温度 d.适度增大压强 e.及时分离出产物f.对原料进行循环利用 g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 j.工厂地址可选择在盛产天然气的地区
设备Ⅰ的名称____________。工业产生中为了节约资源、降低成本和保护环境,常常对某些物质进行循环利用。上述转化关系中能达到该目的的是____________(填序号)。
(3)现有1 mol A参加反应,假设各步均完全反应,生成N的质量为1 165 g,生成K的质量为224 g,则反应①化学反应方程式为____________________。
A~O等十五种物质之间的转化关系如下图所示。A可作为工业生产J的原料,B、C、H、I为非金属单质,X的水溶液在甲型HlNl 流感的防治中常用作消毒液,D在常温下是无色液体且与X的组成元素相同。F为常见的红棕色防锈油漆颜料的主要成分,O是含氮量最高的常见氮肥,且反应⑦中L与M 的物质的量之比为l︰2,A、E、J、N 中含有同一种元素。
回答下列问题:
⑴写反应的化学方程式①___________________________;②________________________;③ ________________________;⑦_______________________________________。
⑵ 步骤⑥的目的和作用________________,设备I中的反应温度是____________(l分),这主要是由________________所决定的(l分)。
⑶组成B、C、I三种单质的非金属元素的气态氢化物的沸点由高到低的顺序是:(用化学式填写) ________________________________________________________________。

| ||
| ||
| ||
| 高温高压 |
| ||
| 高温高压 |
| ||
| ||
| ||
| ||
一、选择题(本题包括6小题,每小题4分,共24分。每小题只有一个选项符合题意)
1.B 2.C 3.B 4.A 5.D 6.A
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
7.AD 8.D 9.B 10.AC 11.BD 12.C 13.D 14.A 15.BC
三.(本题包括2小题,共22分)
16.⑴cd ⑵①硫酸溶液、氢氧化钾溶液 ②1┱4
(除第⑴小题4分外,其余每空2分,共8分)
17.⑴①溶液蓝色恰好褪去所需的时间,吸收前后颗粒吸附剂、棉花、盛放容器的总质量
②同时加入少量碘化钾固体,用适量水使之完全溶解 将第一步所得溶液全部转入1000mL的容量瓶中,定容,摇匀
⑵①800 ②抽气速度过快,或装置气密性较差
③将50mL5×10-4mol/L的碘溶液的体积减小为5mL,并将广口瓶改为试管
⑶④ (每空2分,共14分)
四.(本题包括3小题,共30分)
18.⑴第三周期、ⅠA族 ⑵①C+4HNO3(浓)CO2↑+4NO2↑+2H2O
②2Na2O2+2CO2=2Na2CO3+O2 ⑶ (每空2分,共8分)
19.⑴①该晶体是分子晶体,各分子间存在较弱的分子间作用力,故“可燃冰”熔沸点较低
②890.3 kJ?mol-1
⑵①O2+4e=2 O2? 向负极移动 ②固体碳(或炭粒)
⑶寻找新能源,提高燃料的燃烧效率等
(每空2分,共12分)
20.⑴H2O2 ⑵acdefgj 合成塔 ⑥ ⑶Fe4S5+8O22Fe2O3+5SO2
(除第⑵小题第2、3空1分外,其余每空2分,共10分)
五.(本题包括2小题,共20分)
21.⑴乙基 C9H12O3 ⑵与NaOH溶液在加热条件下反应
⑶ (每空2分,共8分)
22.⑴加成反应 ⑵⑥ 保护B(或G)分子中的C=C不被氧化
⑶
⑷ HOOCCH2CHClCOOH+3NaOHNaOOCCH=CHCOONa+NaCl+3H2O
2CH3CH2CH2CH2OH+HOOCCH=CHCOOH
CH3(CH2)3OOCCH=CHCOO(CH2)3CH3+2H2O (每空2分,共12分)
六.(本题包括2小题,共18分)
23.⑴CaCO3?MgCO3 (4分)
⑵由于炭粉过量,则白云石分解后的产物与炭粉反应完全,据氧元素守恒知,CaCO3?MgCO3→6CO,则V ==0.73am (4分)
24.⑴设乙烯总量为1mol,第①步反应消耗乙烯为xmol,则第②步产生的CH3COOH为x?75%×80%=0.6x。
由反应③知:=
即:x= 1-x=
故两次投料比为=x:(1-x)=5:3。 (4分)
⑵n(CH2=CH2)==1×106mol
m(CH3COOCH=CH2)=1×106mol××75%×86g/mol=2.42×107g=2.42×104kg(3分)
⑶ 第①步消耗氧气:n(O2)1=n(CH2=CH2)××=n(CH2=CH2)
第②步消耗氧气:n(O2)2=n(CH2=CH2)××75%×=n(CH2=CH2)
第③消耗氧气:n(O2)3=n(CH2=CH2)×=n(CH2=CH2)
n(O2)总=n(CH2=CH2)+n(CH2=CH2)+n(CH2=CH2)=n(CH2=CH2)
n(空气)=5×n(CH2=CH2)=n(CH2=CH2)
故:= (3分)
注:答题中出现的其它合理答案均给分
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com