
题目列表(包括答案和解析)
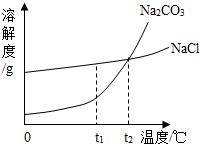 我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如下图所示,据图回答下列问题:
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如下图所示,据图回答下列问题: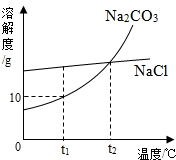 我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
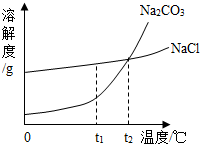
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl)。Na2CO3和NaCl的溶解度曲线如下图所示。据图回答下列问题:
(1)t1℃时,溶解度较大的物质是__ ①______。
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得__②___的碳酸钠溶液(填“饱和”或“不饱和”)。
|
(4)将3克 NaCl固体配成15%的NaCl溶液,
需要加水 ④ mL(水的密度为1g/cm3)。在用量筒
量取水的体积时,如采用右图所示的方法读取数据
(其它操作均正确),则所得溶液中溶质的质量分数
⑤ 15%(选填“<”、“>”或“=”)。


一、选择题(共25个小题,每个小题1分,共25分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
A
A
B
D
D
C
D
C
B
A
C
A
C
题号
14
15
16
17
18
19
20
21
22
23
24
25
答案
D
B
B
A
B
D
C
C
D
A
D
B
二、填空题(共5个小题,共30分)
26.(共9分,每空1分)
/2009年北京市延庆县第一学期期末统测初三化学.files/image068.gif) (1)Al O H (2)FeCl3 +4
(1)Al O H (2)FeCl3 +4
(3)B C H2、O2(或Cl2) 2H2+O2 2H2O
27.(共5分,每空1分)
(1) D
(2) 生成物为CO2和H2O,不污染空气
/2009年北京市延庆县第一学期期末统测初三化学.files/image069.gif)
(3)2H2O 2H2↑+O2↑ (4) N2 (5)A、B、C
28.(共5分,每空1分)
(1) 氯化钠(或NaCl) (2) 饱和
(3) 碳酸钠溶解度随温度降低而明显降低,冬天温度低,溶解在水中的碳酸钠就析出,所以冬天可捞碱。 (4) 25 <
29.(共5分)
(1)下降 镁与稀硫酸反应放热,致使瓶内气压大于外界气压(合理即给分)
(2) B、C
(3) ①化学反应常伴有能量变化 ②分子之间有间隔 (2分)(合理即给分)
30.(共6分)
(1)O2 熟石灰
(2)CO2 + Ca(OH)2 == CaCO3↓+ H2O CO + H2O = H2CO3
(3) C、H(或H、Cl) (2分,答对1种元素给1分)
三、实验题(共3个小题,共19分)
/2009年北京市延庆县第一学期期末统测初三化学.files/image070.gif) 31.(共8分,每空1分)
31.(共8分,每空1分)
(1) 锥形瓶 (2)A B 2H2O2 2H2O+O2↑
(3) b、c、d、a
(4) CaCO3+2HCl→CaCl2+H2O+CO2↑; C ①③
32.(共5分,每空1分)
密度比空气密度大、不能燃烧、不能支持燃烧(三点答全得1分)
(1)杯内的氧气被耗尽,同时又产生了不能燃烧且不能支持燃烧的气体。(合理即给分)
蜡烛燃烧产生的CO2密度大,会下沉。 高的
(2)①②
33.(共6分,每空1分)
【实验设计】 氧气(或O2) ;
增加水中的氧气含量,供鱼苗呼吸
【实验反思】 氧化钙与水反应,生成氢氧化钙。或CaO+H2O→Ca(OH)2
实验步骤
实验现象
结论
取反应后所得溶液样品于试管中,然后通入CO2气体。
产生白色沉淀(或溶液变浑浊)
2CaO2+2H2O→2Ca(OH)2+O2↑
四、计算题(共2个小题,每小题3分,共6分。最后结果保留一位小数)
34.(共3分,每空1分)
(1) 6∶1 ; 66.7% (2)
35.(共3分)
【解】设:生成次氯酸钠的质量为X,氢气的质量为y
MNaCl ==11.7%×
/2009年北京市延庆县第一学期期末统测初三化学.files/image071.gif) 则:NaCl+H2O
NaClO+H2↑
则:NaCl+H2O
NaClO+H2↑
58.5 74.5 2
/2009年北京市延庆县第一学期期末统测初三化学.files/image072.gif)
|