
题目列表(包括答案和解析)
| 加热 |
| 加热 |

| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 |
①有白色沉淀生成 ②溶液由无色变为红色 |
猜想③正确 |
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 问题1:小纸袋中的物质 能否继续作干燥剂? |
取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁. | 不发热 不发热 |
不能作 干燥剂 |
| 问题2:我猜想变质后的物质可能是 CaCO3 (或碳酸钙) CaCO3 (或碳酸钙) |
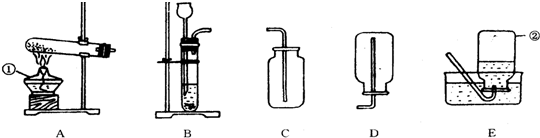
取小纸袋中少量固体于试管中,注入稀HCl 取小纸袋中少量固体于试管中,注入稀HCl (可图示) |
有气泡产生 有气泡产生 |
固体中有碳酸钙 固体中有碳酸钙 |
| 不同的时间段 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
| 鸡蛋壳和稀盐酸的质量/g | 115.0 | 112.8 | 110.6 | 110.6 |
| 生成气体的质量/g | 0 | 2.2 | 4.4 | 4.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com