
题目列表(包括答案和解析)

![]()


上述反应中,关于(Ⅰ)、(Ⅱ)两步的反应类型,正确的是( )
A.化合反应,分解反应 B.加成反应,水解反应
C.还原反应,分解反应 D.氧化反应,水解反应
(2)在上述化合物中,左旋多巴(C)属于氨基酸,它具有两性,即:既有酸性,又在
碱性。因此,它们只是与下列物质中的( )不进行反应。
A.金属钠 B.氢氧化钠 C.氯化钠 D.盐酸




| 浓硫酸 |
| △ |
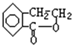 +H2O
+H2O
| 浓硫酸 |
| △ |
 +H2O
+H2O

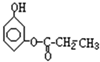





(11分)在Ar、KCl、CO2、SiO2、NaOH等物质中[(1)题填物质的名称]
(1)构成各物质的微粒中,只存在离子键的是____ ;只存在共价键的是______ _;既存在离子键又存在共价键的是_____ ____;不存在化学键的是______ ___。
(2)在上述化合物中,固态时属于原子晶体的是____ ;属于分子晶体的是_____ __属于离子晶体的是____ ____。
(3)KCl的电子式是_______ _,CO2的电子式是____ ____。
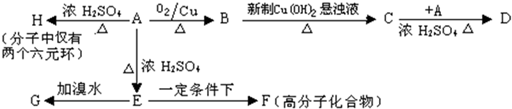
某芳香族化合物A的分子式为C9H10O3,它有两个邻位取代基,A―H有如下的转化关系:
(1)写出B中所含官能团的名称 。
(2)在上述化合物中,可能作酯类的是 。(填写化合物的字母)
(3)写出A→E的化学方程式 ,反应类型为 。
(4)写出2个符合下列要求的A的同分异构体的结构简式: 。
①3个取代基处于间位,且3个取代基各不相同;
②该物质遇FeCl3溶液显紫色,且能发生银镜反应和水解反应。
巩固:1、B 2、.(1) ③ (2)甲烷 ②(3)③ 氢气的输送和贮存
3、 2 3 2 4、B
5、(1)B(CH3)3+2HBr B(CH3)Br2+2CH4
B(CH3)Br2+2CH4
(2)n[B(CH3)3]= n(HBr)=
n(HBr)=
设生成B(CH3)2Br为a mol B(CH3)Br2为b mol

 则:
a+b=
则:
a+b=
a+2b=0.12 b=0.02mol
∴n[B(CH3)Br]:n[B(CH3)Br2]=4:1
随堂作业:
1、C 2、C 3、B 4、C 5、C 6、B 7、C 8、B 9、C 10、C
11.(1)3.5 (2)+3,-3 (3)SiC
12、(1)H++OH-=H2O,使平衡向脱矿方向移动 (2)5Ca2++3PO +F-=Ca5(PO4)
+F-=Ca5(PO4)
(3)加Ca2+ 或加PO ,或其它合理的方法
,或其它合理的方法
13、(1)K= (2)大于 (3)C10H14N2
(2)大于 (3)C10H14N2
14、(1)2CO+2NO 2CO2+N2 (2)SO2转化为SO3,产生硫酸酸雾 (3)a b
2CO2+N2 (2)SO2转化为SO3,产生硫酸酸雾 (3)a b
15、(1)3H2S+2Fe(OH)3→Fe2S3+6H2O
(2)27n (3)b
(4)生产纯碱(或作制冷剂等,其它合理答案也给分)
(5)
16、(1)钡的质量为
(2)原子个数比为Ba:Fe:O=1:2:4,化学式为BaFe2O4(或BaO?Fe2O3)
17、(1)23.3%
(2)1.26×1018 千焦 (3)A= 千克 Q为每生成1摩尔葡萄糖所需要吸收的能量(或:每消耗6摩尔CO2所需吸收的能量)
千克 Q为每生成1摩尔葡萄糖所需要吸收的能量(或:每消耗6摩尔CO2所需吸收的能量)
18.解:(1)35.5/(12×2+1×3+35.5)×100%=56.8%
(2)1吨聚乙烯:1吨×(12×2+1×3+35.5)/(12×2+1×2)=2.4吨聚氯乙烯
(3)50年×2.4=120年
(4)计算表明,与其他通用塑料不同,聚氯乙烯含56.8%的氯,可以大量节约天然资源。可见聚氯乙烯虽然存在不足,但也有不少优点,因此对聚氯乙烯的使用要一分为二,即:既要充分利用,发挥其优点,节约资源;又要注意使用方法,如避免在一次性情况下使用聚氯乙烯因为焚烧回收的能源少,且污染环境,避免使用聚氯乙烯制品装食物、药品、日用品等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com