
题目列表(包括答案和解析)
化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验
(一)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验:
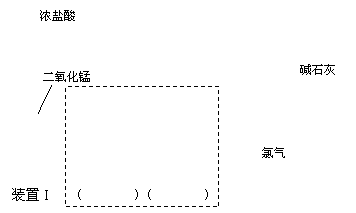

①烧瓶中发生反应的离子方程式为: ;
②请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;

 (二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
(二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
①检查制取氢气装置气密性的操作方法是
②当点燃氢气后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
③试管中加入少量CuSO4溶液的作用是 ,其原理是
(三)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验,A组同学发现制取氢气后的试管中还有较多固体剩余。同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生。请解释可能原因(用离子方程式表示):
;B组同学向集气瓶中注入适量水,用力振荡后,向其中滴入少量Na2S2O3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。(已知Na2S2O3+ H2SO4= Na2SO4+S↓+SO2↑+ H2O),同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①
②
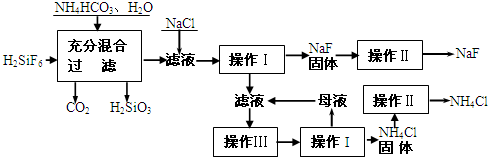
| 温度 | 10℃ | 20℃ | 30℃ | 溶解度:20℃NaF-4g;0℃NH4F-100g; 常温Na2SiF6-微溶于水 |
| NH4Cl溶解度 | 33.3g | 37.2g | 41.4g |
(20分)某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计右图所示装置进行“铁与水反应”的实验。

(1)硬质试管中发生反应的化学方程式为 。
(2)反应前A中投放碎瓷片的目的是 。
(3)装置E中的现象是 。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质试管B冷却后,取少许其中的固体物质溶于 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同) 。;若溶液未变红色,推断硬质玻璃管B中固体物质的成分
①一定有Fe3O4,可能有Fe ②Fe3O4和Fe ③只有Fe3O4 ④只有Fe
(6)另一份用___ (填仪器名称)加入 ,可以证明溶液中存在Fe2+。
【探究三】设计如下流程利用上述滤液制取绿矾晶体(FeSO4·7H2O)。
滤液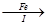 FeSO4溶液
FeSO4溶液 FeSO4·7H2O晶体
FeSO4·7H2O晶体
(7)步骤I中加入洁净废铁屑的作用是 (用化学方程式表示)。
(8)步骤II从FeSO4稀溶液中得到FeSO4·7H2O晶体的主要操作包括 、趁热过滤____、再过滤。为防止FeSO4变质,该流程中还需注意的问题有 。
【探究四】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
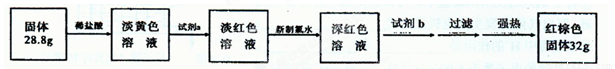
(9)试剂b的化学式是 ____。
(10)计算反应后B装置中铁元素的质量分数为 ;根据计算结果判断反应后硬质试管B中固体物质的成分是 。
(20分)某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计右图所示装置进行“铁与水反应”的实验。
(1)硬质试管中发生反应的化学方程式为 。
(2)反应前A中投放碎瓷片的目的是 。
(3)装置E中的现象是 。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质试管B冷却后,取少许其中的固体物质溶于 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同) 。;若溶液未变红色,推断硬质玻璃管B中固体物质的成分
①一定有Fe3O4,可能有Fe ②Fe3O4和Fe ③只有Fe3O4 ④只有Fe
(6)另一份用___ (填仪器名称)加入 ,可以证明溶液中存在Fe2+。
【探究三】设计如下流程利用上述滤液制取绿矾晶体(FeSO4·7H2O)。
滤液![]() FeSO4溶液
FeSO4溶液![]() FeSO4·7H2O晶体
FeSO4·7H2O晶体
(7)步骤I中加入洁净废铁屑的作用是 (用化学方程式表示)。
(8)步骤II从FeSO4稀溶液中得到FeSO4·7H2O晶体的主要操作包括 、趁热过滤____、再过滤。为防止FeSO4变质,该流程中还需注意的问题有 。
【探究四】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
(9)试剂b的化学式是 ____。
(10)计算反应后B装置中铁元素的质量分数为 ;根据计算结果判断反应后硬质试管B中固体物质的成分是 。
(20分)某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计右图所示装置进行“铁与水反应”的实验。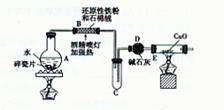
(1)硬质试管中发生反应的化学方程式为 。
(2)反应前A中投放碎瓷片的目的是 。
(3)装置E中的现象是 。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质试管B冷却后,取少许其中的固体物质溶于 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同) 。;若溶液未变红色,推断硬质玻璃管B中固体物质的成分
①一定有Fe3O4,可能有Fe ②Fe3O4和Fe ③只有Fe3O4 ④只有Fe
(6)另一份用___ (填仪器名称)加入 ,可以证明溶液中存在Fe2+。
【探究三】设计如下流程利用上述滤液制取绿矾晶体(FeSO4·7H2O)。
滤液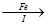 FeSO4溶液
FeSO4溶液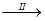 FeSO4·7H2O晶体
FeSO4·7H2O晶体
(7)步骤I中加入洁净废铁屑的作用是 (用化学方程式表示)。
(8)步骤II从FeSO4稀溶液中得到FeSO4·7H2O晶体的主要操作包括 、趁热过滤____、再过滤。为防止FeSO4变质,该流程中还需注意的问题有 。
【探究四】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。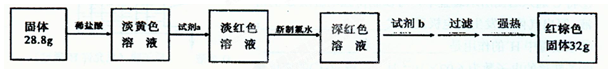
(9)试剂b的化学式是 ____。
(10)计算反应后B装置中铁元素的质量分数为 ;根据计算结果判断反应后硬质试管B中固体物质的成分是 。
15、(10分)
⑴结构式(1分);测定pH 或滴加Na2CO3溶液 或将甲酸滴加到滴有酚酞的NaOH溶液中(不能用Na,其它合理答案均可得分)(2分)
⑵(2分)测定HCOONa溶液的pH;或将等pH的HCOOH溶液和HCl溶液稀释相同倍数,测其pH的变化;或比较等浓度甲酸和盐酸的导电性等(合理均可给分)
⑶(2分)出现银镜,由于羟基对醛基的影响,导致甲酸中的醛基不具有典型醛基的性质(1分。羧基中C原子和2个O原子之间形成1个大л键,而使甲酸分子中的醛基性质不太典型);或答稀氨水量不足,使甲酸与银氨溶液混合后仍显酸性(1分)
⑷ ① 甲酸在浓硫酸的作用下脱水生成CO和H2O(1分)
 ②(2分)
②(2分)
16、(8分 每空1分)
 (1)
离子键、共价键(或非极性键)
(1)
离子键、共价键(或非极性键)
(2)FeS2 -1 (3)Fe2O3+6H+=2Fe3++3H2O Fe2(SO4)3+6KOH=2Fe(OH)3↓+3K2SO4
(4)Cu-2e=Cu2+ (5) 852
17. (12分)(1)SO2+NaOH=NaHSO3 (1分) HSO3-+H+==SO2+H2O (1分)
 (2) AB
(2分) 实验时间和加入盐酸酸化的氯化钡溶液后生成沉淀的质量 (2分)
(2) AB
(2分) 实验时间和加入盐酸酸化的氯化钡溶液后生成沉淀的质量 (2分)
 (3)变废为肥,充分利用资源,降低污染 (2分)
(3)变废为肥,充分利用资源,降低污染 (2分)
 (4)+4 (2分)
(4)+4 (2分)
 (5)5CH3OH+6NO3--+6H+ ==5CO2+3N2+13H2O (2分)
(5)5CH3OH+6NO3--+6H+ ==5CO2+3N2+13H2O (2分)
18.(共8分,每空2分)
(1)3NaClO3+3H2SO4=2ClO2↑+HClO4+H2O+3NaHSO4
或 3NaClO3+2H2SO4=2ClO2↑+NaClO4+H2O+2NaHSO4
(2)二氧化硫作为还原剂把ClO2还原为NaClO2
2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O
(3)H2SO4
19.(12分)


 ⑴
(或
),
(2分,各1分)
⑴
(或
),
(2分,各1分)
 ⑵
(2分)
⑵
(2分)

(3分)
⑶ ④、⑤、⑥ (写对一个得一分,错一个扣一分,扣完为止,3分)
⑷ ①、③ (2分,各1分)
20. (10分)(1).2.8×105 ;18
(2).86.96% (3). ;138
;138
21、(12分)⑴分子 (2分) 1s2s22p63s23p63d84s2或[Ar]3d84s2 (2分)
⑵ACD (2分) ⑶①、③、④ (2分) 平面三角 (2分)
⑷LaNi5或Ni5La (2分)
I.将0.050molSO2和0.030molO2放入容积为 2SO3(g)
;△H=-196.6kJ?mol-1,恒温恒容下达到平衡时,测得容器A中放出3.932 kJ的热量,则容器A中SO2的平衡转化率为
;容器B中SO2的平衡转化率(填“大于”、“小于”或“等于”)
2SO3(g)
;△H=-196.6kJ?mol-1,恒温恒容下达到平衡时,测得容器A中放出3.932 kJ的热量,则容器A中SO2的平衡转化率为
;容器B中SO2的平衡转化率(填“大于”、“小于”或“等于”)
容器A中SO2的平衡转化率;达到平衡的时间(填“A”或“B”) 容器比较短;
II.滴定分析法是化学分析法中的重要分析方法之一。滴定分析法就是将一种已知准确浓度的试剂溶液(即标准溶液),由滴定管滴加到被测定的物质的溶液(即试液)中,直到化学反应完全时为止,然后根据所用试剂溶液的浓度和体积,就可以求得被测组分的含量。
(1) 已知用0.10 mol/L HCl滴定 20.00ml
0.10 mol/L Na2CO3的滴定曲线如右图所示:
 ① A处选用
作指示剂比较合适;
① A处选用
作指示剂比较合适;
② 当滴定至混合液pH接近4时,为了防止
终点出现过早,减少实验的误差,应剧烈地
摇动溶液或加热一会溶液,冷却后再继续滴
定,这样做的理由是:
;
如果是采用加热溶液的操作,应如何进行?
;
(2)(2)EDTA是乙二胺四乙酸的英文名称的缩写,
它是一种常用的滴定剂,市售试剂是其二水合二钠
盐。下表是EDTA与一些常见金属离子形成络合物
(用MY表示)的稳定常数(温度25oC):
阳离子
lgKMY
阳离子
lgKMY
Na+
1.66
Mn2+
13.87
Ca2+
10.96
Pb2+
18.04
lgKMY值越大,表明金属离子与EDTA形成的络合物越稳定,越难电离
根据上表给出的数据和你所学的知识,解释为什么用CaY溶液可以排除体内的铅?
___________________________________________________________________________。
23.(12分)
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究。
[实验一]为测定硫元素的含量
Ⅰ.将m 2Fe2O3+8SO2
2Fe2O3+8SO2
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
问题讨论:
⑴.Ⅰ中,甲瓶内所盛试剂是________溶液。乙瓶内发生反应的离子方程式有_________________、_________________。
⑵.Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是_____________。
⑶.该黄铁矿中硫元素的质量分数为______________。
[实验二]设计以下实验方案测定铁元素的含量

问题讨论:
⑷.③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有__________。
⑸.②中,若选用铁粉作还原剂,你认为合理吗?理由是:____________。
五、(本题包括1小题,9分)
25.(9分)
咖啡酸苯乙酯 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化:
请填写下列空白。
⑴.D分子中的官能团是________。
⑵.高分子M的结构简式是______________。
⑶.写出A→B反应的化学方程式:___________________。
⑷.B→C发生的反应类型有______________。
⑸.A的同分异构体很多种,其中,同时符合下列条件的同分异构体有____种。
①苯环上只有两个取代基;
②能发生银镜反应;
③能与碳酸氢钠溶液反应;
④能与氯化铁溶液发生显色反应。
(10分)已探明我国锰矿储量占世界第三位,但富矿仅占6.4%,每年尚需进口大量锰矿石。有人设计了把我国的贫菱锰矿(MnCO3含量较低)转化为高品位“菱锰矿砂”(MnCO3含量高)的绿色工艺。该工艺流程如下图所示:

已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3MnSO4+2NH3↑+CO2↑+H2O。
(1)写出反应②的离子方程式_______________________________________。
(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、____________、__________。从物料平衡角度看,理论上生产过程中_________(填“需要”或者“不需要”)添加(NH4)2SO4。
(3)向物质的量浓度均为0.01mol?L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是________(填离子符号);当两种沉淀共存时,溶液中 =________。
=________。
[Ksp(BaCO3)=8.1×10-9,Ksp(MnCO3)=1.8×10-11]
(10分)(1)Mn2++2NH3+CO2+H2O=2NH4++MnCO3↓(2分)
(2)NH3、CO2 (2分) 不需要(2分)
(3)Mn2+(2分) 450(2分)
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com