
题目列表(包括答案和解析)
 某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算:
某兴趣小组测定贝壳中CaCO3的含量.现取l2g贝壳捣碎,放入烧杯中,然后向其中加入73g某质量分数的稀盐酸,使之充分反应(贝壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用稀盐酸刚好消耗了加入量的一半.试计算: 鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数).
鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数).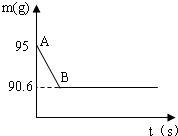 鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好完全反应.试计算(计算结果保留1位小数):
鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好完全反应.试计算(计算结果保留1位小数):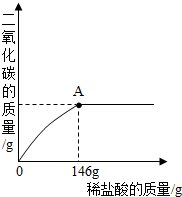 现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:
现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2不与空气中主要成分反应,且 密度比空气大 密度比空气大 |
| 收集验满过程分析 | 集满的现象是:集气瓶内液面降至瓶口,且有 气泡 气泡 从瓶口逸出 |
集满的现象是:用燃烧的木条放在瓶口,燃烧的木条 熄灭 熄灭 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com