
题目列表(包括答案和解析)
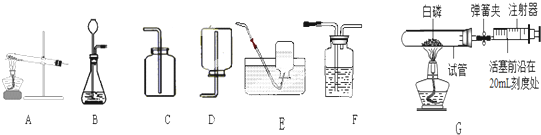
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 |
| ②另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴 |
溶液中有大量气泡放出 |
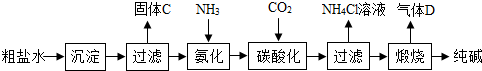
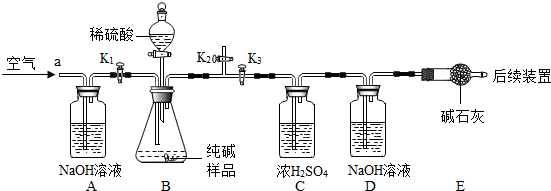
根据下列装置图,回答有关问题:
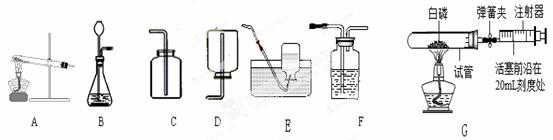
(1)实验室用装置B制取氧气时,收集装置可选用 ▲ ,写出反应的化学方程式 ▲ ;如用注射器替换长颈漏斗,优点是 ▲ ; 要得到一瓶干燥的氧气,所选装置连接顺序是 ▲ (填装置大写字母),可选用 ▲ 作干燥剂 。
。
(2)注射器可用于检查装置B的气密性,步骤如下:
①向锥形瓶中加入少量水至 ▲ 处.
②将注射器连接到装置B的导管口处.
③缓慢拉动注射器的活塞,观察到 ▲ ,表示装置B气密性良好.
(3)图G实验中(铁架台略去)操作步骤如下:
①点燃酒精灯.
②读取活塞数据.
③撤去酒精灯,待试管冷却后松开弹簧夹.
④将少量红磷平装入试管中,将活塞置于20mL刻度处,并按图G中所示连接方式固定好,再将弹簧夹紧橡皮管.
⑤检查装置气密 性.
性.
你认为正确实验操作顺序是 ▲ (填序号).
(4)图G实验中(选用容积为40mL的试管作反应容器),活塞将从20mL刻度处慢慢前移到约为 ▲ mL刻度处才停止.
(5 )实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解。CuSO4
)实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解。CuSO4 溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用。小红同学作了以下分析和设计。
溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用。小红同学作了以下分析和设计。
①小红同学认为最不可能的是H2O,她的理由是 ▲ 。
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液几乎没有气泡放 | 实验证明,起催化作用的是 ▲ 。 |
| ②另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴 ▲ | 溶液中有大量气泡放出 |
③如果确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后
▲ 。
| ||
| ||
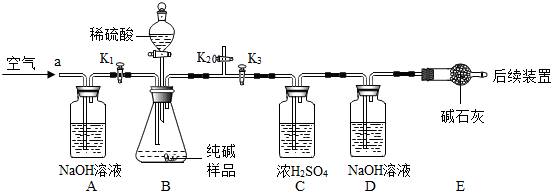
| 106 |
| 10.6g |
| 44 |
| x |
| 106 |
| 10.6g |
| 44 |
| x |
| 编号 | 所加的物质 | 温度 | pH | 变色情况 | |
| A | 80mL蒸馏水 | 20g葡萄糖 | 22℃ | 7 | 28天后呈极浅黄色 |
| B | 80mL自来水 | 20g葡萄糖 | 22℃ | 6.8 | 6天后呈极浅黄色 |
| C | 80mL矿泉水 | 20g葡萄糖 | 22℃ | 7.1 | 13天后呈极浅黄色 |
| D | 80mL蒸馏水 | 5g葡萄糖 | 22℃ | 7 | 60天后仍无明显变化 |
| E | 80mL蒸馏水 | 30g葡萄糖 | 22℃ | 7 | 18天后呈极浅黄色 |
| F | 80mL蒸馏水 | 20g葡萄糖 | 0℃ | 7 | 60天后仍无明显变化 |
| G | 80mL蒸馏水 | 20g葡萄糖 | 60℃ | 7 | 12天后呈极浅黄色 |
| H | 80mL蒸馏水+1mL稀硫酸 | 20g葡萄糖 | 22℃ | 3 | 60天后仍无明显变化 |
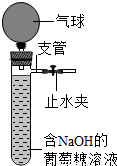
| I | 80mL蒸馏水+1mL氢氧化钠溶液 | 20g葡萄糖 | 22℃ | 11 | 7分钟后呈极浅黄色 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com