
题目列表(包括答案和解析)

| ||
| ||
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,滴加 Ca(OH)2溶液 Ca(OH)2溶液 |
生成白色沉淀 生成白色沉淀 |
该氢氧化钠溶液已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加入足量的 CaCl2 CaCl2 溶液,过滤,在滤液中滴加无色酚酞 无色酚酞 溶液 |
产生白色沉淀 溶液变红 溶液变红 |
该氢氧化钠 部分 部分 变质(填“部分”或“全部”) |
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.
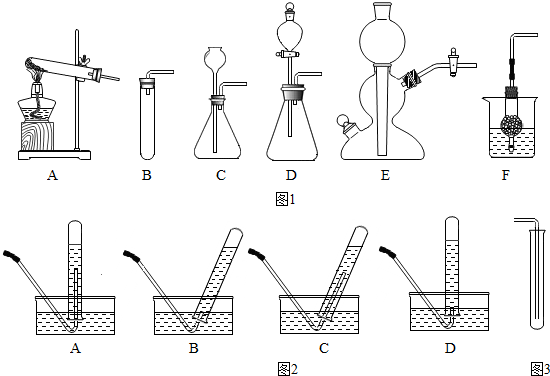
步骤一:选取药品与反应装置.实验室经常选用稀盐酸和 (填药品名称)作为反应物制取二氧化碳气体,发生反应的化学方程式为: .发生装置除了选择B以外,还可选用图1中的C、D、E或F.装置E或F相对于装置C在操作方面的优势为: .
步骤二:检查装置气密性.若选择B作为气体的发生装置,组装好仪器后,将导管末端浸末在水中,用手握住试管,发现导管口 ,则气密性良好.
步骤三:反应并收集气体.在小试管中,用排水法和向上排空气法各收集一试管二氧化碳.用排水法收集二氧化碳,图2装置正确的是 ,判断气体已集满的现象是: .
用向上排空气法收集二氧化碳(装置如图3),可将燃着的小木条放在 来验满.
步骤四:检验二氧化碳气体.
(1)向两根收集好二氧化碳的试管中,均注入约占试管三分之一体积的澄清石灰水,旋紧胶塞,同时用力上、下振荡,小明同学观察到两根试管中的液体都变浑浊,且用排水法收集的试管中更浑浊,说明用 收集的气体纯度更高,发生的反应用化学方程式表示是: .
(2)排水法比排空气法收集的气体更纯的原因是: .
A.排水法收集时,导管口一有气泡就开始收集气体
B.排空气法收集,验满时当燃着的木条熄灭,说明二氧化碳的浓度较大,并不代表是纯净的二氧化碳气体
C.气态分子间隔大,运动速度快,不同气体分子更易混合,不易分离,二氧化碳很难将空气排干净
D.排空气法收集的气体中,会混有少量的氯化氢气体(从盐酸中挥发出来的)

 (2009?广元)某学生为测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已略去),实验在
(2009?广元)某学生为测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已略去),实验在湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com