
4、 了解用基准物质来标定标准溶液
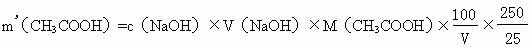 则100mL食醋中所含醋酸的质量为
则100mL食醋中所含醋酸的质量为
3、 课题方案设计
(1) 配制待测食醋溶液:用25mL移液管吸取食醋25mL,在容量瓶中配制250mL的食醋溶液。
(2) 将样品装入酸式滴定管:酸式滴定管用待测食醋润洗3次,然后装入食醋溶液。
(3) 把标准NaOH溶液装入碱式滴定管
(4) 取待测液:从酸式滴定管中放出VmL待测食醋到洗净的锥形瓶中,加2~3滴酚酞溶液。
(5) 滴定:左手控制滴定管的玻璃球,右手振荡锥形瓶,两眼注视锥形瓶内溶液颜色的变化,当锥形瓶内溶液颜色从无色到浅红色且半分钟内不恢复到原来的颜色,说明滴定到终点。
(6) 数据处理:m(CH3COOH)=c(NaOH)×V(NaOH)×M(CH3COOH)
2、 食醋的总酸含量:是指每100mL食醋中含酸(以醋酸计)的质量,也称食醋的酸度。
1、 食醋的分类:分为酿造醋和配制醋
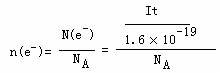
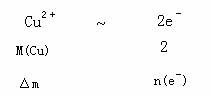
专题六:物质的定量分析
课题17:食醋总酸含量的测定(用已知浓度的NaOH溶液滴定待测食醋样品溶液,可测定食醋总酸含量)
电镀液的配制:50mL蒸馏水+3.5gZnCl2+12.5gKCl+
(若PH>6,则易生成白色絮状的氢氧化物沉淀以及锌的碱式盐,若PH<5,镀液中的H+浓度大,一方面会造成H+和Zn2+对配位体Cl-的争夺,另一方面,由于H+浓度大,易放电,形成的氢气气泡附着在阴极表面而影响镀层质量)。
镀件的处理:用细砂纸打磨铁钉,使铁钉光滑→放在
电镀操作:Zn(阳极),Fe(阴极),电渡液进行电镀。
课题15:阿伏加德罗常数的测定
测定物理量:电极物质的质量(△m),通过电解液的电流强度(I)和通电时间(t)
2、铁钉镀锌
1、 电解饱和食盐水
取一支U型管,向管内加入饱和食盐水,并滴入几滴酚酞,用铁棒和碳棒分别作为阴极和阳极,接上直流电源进行电解。
现象:在阳极收集到Cl2,用湿润的KI-淀粉试纸检验显蓝色。
阴极收集到H2(可用点燃检验),阴极由于H+的消耗,OH-剩余呈碱性,酚酞变红。
课题14、电解和电镀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com