
16ЃЎ(2010ЁЄЬкГхФЃФт)ЯТСаЭМЪЧвЛИіЪЕбщЪОвтЭМЃЌЗНПђБэЪОгаЙиЕФвЧЦїЃЌМ§ЭЗБэЪОвКЬхЛђЦјЬхЕФСїЯђЁЃ
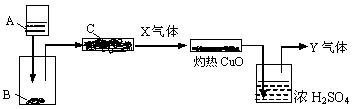
ЭМжаAЪЧвКЬхЃЌBЁЂCЪЧЙЬЬхЁЃAгыBЗДгІКѓВњЩњЕФЦјЬхОЙ§CЃЌЕУЕНДПЦјЬхXЁЃXЭЈЙ§зЦШШCuOЃЌCuOзЊЛЏЮЊCuЁЃЦјЬхдйЭЈЙ§ХЈH2SO4ЃЌзюКѓЕУЕНДПЦјЬхYЃЌYЪЧЖдЛЗОГУЛгаЮлШОЕФЦјЬхЃЌДѓСПХХЗХвВУЛгаЮЃЯеЁЃ
ЮЊНјаавдЩЯЪЕбщЃЌЧыДгЯТСаЪдМСЗЖЮЇФкбЁдёКЯЪЪЕФAЁЂBКЭCЃКХЈСђЫсЁЂЯЁСђЫсЁЂХЈЯѕЫсЁЂЯЁЯѕЫсЁЂХЈбЮЫсЁЂЯЁбЮЫсЁЂаПСЃЁЂХЈNaOHШмвКЁЂДѓРэЪЏЁЂМюЪЏЛвЁЂNH4ClЙЬЬхЁЃ
(1)AЪЧ________ЃЌBЪЧ________ЃЌCЪЧ________ЃЌXЪЧ________ЁЃ
(2)аДГіAКЭBЗДгІЕФЛЏбЇЗНГЬЪН________________________________ЁЃ
(3)аДГіXКЭCuOЗДгІЕФЛЏбЇЗНГЬЪН________________________________ЁЃ
[НтЮі]CгІИУЪЧИЩдяМСЃЌБиШЛЪЧМюЪЏЛвЁЃгЩX+CuO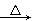 Cu+Y+ЁЃЌCuOБЛЛЙдЃЌЫЕУїXОпгаЛЙдадЃЌНсКЯA+BЁњXЃЌаПСЃКЭХЈСђЫсЁЂХЈЯѕЫсЁЂЯЁЯѕЫсВњЩњЕФSO2ЁЂNO2ЁЂNOМАДѓРэЪЏКЭЯЁбЮЫсВњЩњЕФCO2ВЛФмНЋCuOЛЙдЃЌЫљвдXПЩФмЪЧаПСЃКЭЯЁбЮЫсВњЩњЕФH2ЛђХЈNaOHШмвККЭNH4ClЙЬЬхВњЩњЕФNH3ЁЃШєXЪЧH2ЃЌдђЫќКЭCuOЗДгІКѓЩњГЩЕФЫЎеєЦјФмЙЛБЛХЈH2SO4ЭъШЋЮќЪеЃЌзюКѓВЛПЩФмгаЦјЬхЪЃгрЃЛШєXЪЧNH3ЃЌдђЫќНЋБЛCuOбѕЛЏГЩN2ЃЌЗДгІЩњГЩЕФЫЎеєЦјБЛХЈH2SO4ЭъШЋЮќЪеЃЌзюКѓгаN2ЪЃгрЁЃгЩДЫПЩвдЕУЕНД№АИЁЃ
Cu+Y+ЁЃЌCuOБЛЛЙдЃЌЫЕУїXОпгаЛЙдадЃЌНсКЯA+BЁњXЃЌаПСЃКЭХЈСђЫсЁЂХЈЯѕЫсЁЂЯЁЯѕЫсВњЩњЕФSO2ЁЂNO2ЁЂNOМАДѓРэЪЏКЭЯЁбЮЫсВњЩњЕФCO2ВЛФмНЋCuOЛЙдЃЌЫљвдXПЩФмЪЧаПСЃКЭЯЁбЮЫсВњЩњЕФH2ЛђХЈNaOHШмвККЭNH4ClЙЬЬхВњЩњЕФNH3ЁЃШєXЪЧH2ЃЌдђЫќКЭCuOЗДгІКѓЩњГЩЕФЫЎеєЦјФмЙЛБЛХЈH2SO4ЭъШЋЮќЪеЃЌзюКѓВЛПЩФмгаЦјЬхЪЃгрЃЛШєXЪЧNH3ЃЌдђЫќНЋБЛCuOбѕЛЏГЩN2ЃЌЗДгІЩњГЩЕФЫЎеєЦјБЛХЈH2SO4ЭъШЋЮќЪеЃЌзюКѓгаN2ЪЃгрЁЃгЩДЫПЩвдЕУЕНД№АИЁЃ
[Д№АИ](1)ХЈNaOHШмвКЁЁ NH4ClЙЬЬхЁЁЁЁ МюЪЏЛвЁЁ NH3
(2)NaOH+NH4Cl NaCl+NH3Ёќ+H2OЁЁ
NaCl+NH3Ёќ+H2OЁЁ
(3)2NH3+3CuO 3Cu+N2+3H2OЁЃ
3Cu+N2+3H2OЁЃ
15ЃЎ(2010ЁЄАќЭЗФЃФт)вбжЊХЈH2SO4КЭFe3+ЖМПЩвдНЋCuбѕЛЏ(Fe3+гыCuЕФЗДгІЮЊЃК2Fe3++CuЃН2Fe2++Cu2+)ЃЌХЈH2SO4ЛЙПЩвдНЋBrЃбѕЛЏГЩBr2ЃЌFeгыBr2ЗДгІЩњГЩFeBr3ЃЌдђгаЙиЮяжЪбѕЛЏадЧПШѕЕФЫГађЮЊ(ЁЁЁЁ )ЁЃ
ЁЁ AЃЎH2SO4(ХЈ)ЃОCu2+ЃОFe3+ЃОBr2ЁЁ ЁЁBЃЎH2SO4(ХЈ)ЃОBr2ЃОFe3+ЃОCu2+
ЁЁ CЃЎBr2ЃОH2SO4(ХЈ)ЃОCu2+ЃОFe3+ЁЁЁЁ DЃЎCu2+ЃОFe3+ЃОBr2ЃОH2SO4(ХЈ)
[НтЮі]бЁBЁЃдкбѕЛЏЛЙдЗДгІжаЃЌбѕЛЏМСЕФбѕЛЏадДѓгкбѕЛЏВњЮяЕФбѕЛЏадЃЌОнДЫХаЖЯГіИїИіЗДгІЕФбѕЛЏМСКЭбѕЛЏВњЮяМДПЩЕУЕНД№АИЁЃ
14ЃЎ(2010ЁЄФўВЈФЃФт)аТаЭФЩУзВФСЯбѕШБЮЛЬњЫсбЮ(MFe2Ox)(3ЃМxЃМ4ЃЛMБэЪОMnЁЂCoЁЂZnЛђNiЕФЖўМлРызг)ЃЌГЃЮТЯТЃЌЫќФмЪЙЙЄвЕЗЯЦјжаЕФSO2ЁЂNO2ЕШбѕЛЏЮязЊЛЏЮЊЕЅжЪЁЃзЊЛЏСїГЬШчЭМЫљЪОЃК
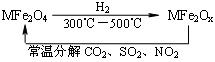
гаЙиЩЯЪізЊЛЏЙ§ГЬЕФЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЃ
ЁЁЁЁ AЃЎMFe2O4БэЯжСЫЛЙдадЁЁЁЁЁЁЁЁ ЁЁBЃЎMFe2OxБэЯжСЫЛЙдад
ЁЁЁЁ CЃЎSO2КЭNO2БэЯжСЫЛЙдадЁЁЁЁЁЁ DЃЎSO2КЭNO2ЗЂЩњСЫЗжНтЗДгІ
[НтЮі]бЁBЁЃMFe2OxФмЪЙSO2ЁЂNO2зЊЛЏЮЊЕЅжЪЃЌМДSO2ЁњSЁЂNO2ЁњN2ЃЌдкИУзЊЛЏЙ§ГЬжаЃЌСђдЊЫиКЭЕЊдЊЫиЕФЛЏКЯМлНЕЕЭЃЌБЛЛЙдЃЌЗЂЩњЛЙдЗДгІЃЌзїбѕЛЏМСЃЌБэЯжбѕЛЏадЃЛдђMFe2OxдкЗДгІжазїЛЙдМСЃЌБэЯжЛЙдадЃЌMFe2O4БэЯжбѕЛЏадЁЃ
13ЃЎ(2010ЁЄдЫГЧФЃФт)ЧІЕФвБСЖДѓжТЙ§ГЬШчЯТЃКЂйИЛМЏЃКНЋЗНЧІПѓ(PbS)НјааИЁбЁЃЛЂкБКЩеЃК2PbS+3O2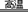 2PbO+2SO2ЃЛЂлжЦДжЧІЃКPbO+C
2PbO+2SO2ЃЛЂлжЦДжЧІЃКPbO+C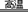 Pb+COЃЛPbO+CO
Pb+COЃЛPbO+CO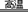 Pb+CO2ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЃ
Pb+CO2ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЃ
ЁЁЁЁ AЃЎИЁбЁЗЈИЛМЏЗНЧІПѓЕФЙ§ГЬЪєгкЛЏбЇБфЛЏ
ЁЁЁЁ BЃЎЗНЧІПѓБКЩеЗДгІжаЃЌPbSЪЧЛЙдМСЃЌЛЙдВњЮяжЛгаPbO
ЁЁЁЁ CЃЎећИівБСЖЙ§ГЬжаЃЌжЦШЁ1mol PbЙВзЊвЦ2molЕчзг
ЁЁЁЁ DЃЎНЋ1mol PbSвБСЖГЩPbРэТлЩЯжСЩйашвЊ6gЬМ
[НтЮі]бЁDЁЃИЁбЁЗЈИЛМЏЗНЧІПѓЕФЙ§ГЬЪєгкЮяРэБфЛЏЃЌAбЁЯюДэЮѓЃЛЗНЧІПѓБКЩеЗДгІжаЃЌЧІдЊЫиЕФЛЏКЯМлУЛгаЗЂЩњБфЛЏЃЌСђдЊЫиЕФЛЏКЯМлЩ§ИпЃЌБЛбѕЛЏЃЌбѕдЊЫиЕФЛЏКЯМлНЕЕЭЃЌБЛЛЙдЃЌЫљвдЛЙдМСЪЧPbSЃЌбѕЛЏМСЪЧO2ЃЌбѕЛЏВњЮяЪЧSO2ЃЌЛЙдВњЮяЪЧPbOКЭSO2ЃЌBбЁЯюДэЮѓЃЛећИівБСЖЙ§ГЬжаЕФЗДгІЮяЪЧPbSЁЂO2КЭCЃЌЩњГЩЮяЪЧPbЁЂSO2КЭCO2ЃЌзмЗДгІЗНГЬЪНЮЊ2PbS+3O2+C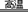 2Pb+2SO2+CO2ЃЌИУЗДгІзЊвЦ12ИіЕчзгЃЌЫљвджЦШЁ1mol PbЙВзЊвЦ6molЕчзгЃЌCбЁЯюДэЮѓЃЛжЦШЁ1mol
PbашвЊ0.5mol CЃЌМД0.5molЁС12g/molЃН6gЃЌDбЁЯюе§ШЗЁЃ
2Pb+2SO2+CO2ЃЌИУЗДгІзЊвЦ12ИіЕчзгЃЌЫљвджЦШЁ1mol PbЙВзЊвЦ6molЕчзгЃЌCбЁЯюДэЮѓЃЛжЦШЁ1mol
PbашвЊ0.5mol CЃЌМД0.5molЁС12g/molЃН6gЃЌDбЁЯюе§ШЗЁЃ
12ЃЎ(2010ЁЄСЩбєФЃФт)НёгаШ§ИібѕЛЏЛЙдЗДгІЃК
ЁЁЁЁ Ђй2FeCl3+2KI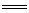 2FeCl2+I2+2KCl
2FeCl2+I2+2KCl
ЁЁЁЁ Ђк2FeCl2+Cl2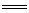 2FeCl3
2FeCl3
ЁЁЁЁ Ђл2KMnO4+16HCl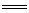 2MnCl2+2KCl+5Cl2Ёќ+8H2O
2MnCl2+2KCl+5Cl2Ёќ+8H2O
ШєФГШмвКжагаFe2+ЁЂIЃКЭClЃЙВДцЃЌвЊбѕЛЏГ§ШЅIЃЖјВЛгАЯьFe2+КЭClЃЃЌПЩМгШыЕФЪдМС
ЪЧ(ЁЁЁЁ )ЁЃ
ЁЁ ЁЁAЃЎCl2ЁЁЁЁ BЃЎKMnO4ЁЁ ЁЁCЃЎFeCl3 ЁЁЁЁDЃЎHCl
[НтЮі]бЁCЁЃИљОнЗДгІЂйПЩЕУбѕЛЏадЃЌFeCl3ЃОI2ЃЌИљОнЗДгІЂкПЩЕУбѕЛЏадЃКCl2ЃОFeCl3ЃЌИљОнЗДгІЂлПЩЕУбѕЛЏадЃКKMnO4ЃОCl2ЃЌдђбѕЛЏадЃКKMnO4ЃОCl2ЃОFeCl3ЃОI2ЃЌБОЬтжавЊбѕЛЏIЃЖјВЛгАЯьFe2+КЭClЃЃЌБиаыбЁбѕЛЏФмСІБШI2ЧПЃЌЖјБШCl2ШѕЕФбѕЛЏМСЃЌжЛгаFeCl3ТњзуЬѕМўЁЃ
11ЃЎ(2010ЁЄеиЧьФЃФт)дкКЌгаFeBr2КЭFeI2ЕФЛьКЯШмвКжаЃЌЭЈШывЛЖЈСПЕФCl2ЃЌдйЕЮМгKSCNШмвККѓЃЌШмвКБфЮЊбЊКьЩЋЃЌдђЛьКЯШмвКжазюгаПЩФмВЛДцдкЕФРызгЪЧ(ЁЁЁЁ )ЁЃ
ЁЁЁЁ AЃЎClЃЁЁЁЁ BЃЎFe2+ЁЁ ЁЁCЃЎIЃЁЁЁЁ DЃЎBrЃ
[НтЮі]бЁCЁЃЕЮМгKSCNШмвККѓЃЌШмвКБфЮЊбЊКьЩЋЃЌЫЕУїШмвКжаКЌгаFe3+ЃЌМДFe2+БЛбѕЛЏЃЌвђЮЊЛЙдадЃКIЃЃОFe2+ЃОBrЃЃЌЫљвдIЃвЛЖЈШЋВПБЛбѕЛЏЃЌШмвКжаВЛПЩФмКЌгаIЃЁЃ
10ЃЎ(2010ЁЄЬЋдФЃФт)дкЯТСаЗДгІЙ§ГЬжаЃЌга3molЕчзгзЊвЦЕФЪЧ(ЁЁЁЁ )ЁЃ
ЁЁЁЁ AЃЎlmolФЦгыЫЎЗДгІ
ЁЁЁЁ BЃЎ27gТСгызуСПбЮЫсЗДгІ
ЁЁЁЁ CЃЎ22.4LбѕЦј(БъзМзДПі)гызуСПУОЗДгІ
ЁЁЁЁ DЃЎ1.5mol Na2O2гызуСПЫЎЗДгІ
[НтЮі]бЁBЁЃЯШБъГіУПИіЗДгІЫљзЊвЦЕчзгЪ§ФПЃЌШЛКѓевГіЕчзгЪ§КЭЫљИјЮяжЪжЎМфЕФЙиЯЕЃЌМДПЩМЦЫуГіИјЖЈСПЕФЮяжЪЫљзЊвЦЕчзгЕФЮяжЪЕФСПЁЃ27gТСКЭБъзМзДПіЯТ22.4LбѕЦјЕФЮяжЪЕФСПЖМЪЧ1molЁЃ
|
бЁЯю |
ФкШнжИЯђЁЄСЊЯЕЗжЮі |
зЊвЦЕчзгЕФЮяжЪЕФСП |
|
A |
2Na+2H2O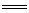 2NaOH+H2Ёќ~2eЃ 2NaOH+H2Ёќ~2eЃ |
1mol |
|
B |
2Al+6HCl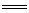 2AlCl3+3H2Ёќ~6eЃ 2AlCl3+3H2Ёќ~6eЃ |
3mol |
|
C |
2Mg+O2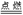 2MgO~4eЃ 2MgO~4eЃ |
4mol |
|
D |
2Na2O2+2H2O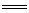 4NaOH+O2Ёќ~2eЃ 4NaOH+O2Ёќ~2eЃ |
1.5mol |
9ЃЎ(2010ЁЄжЃжнФЃФт)ЮЊСЫШЗЖЈЯТСаЮяжЪЪЧЗёБЛбѕЛЏЃЌЫљбЁЪдМС(РЈКХФкЮяжЪ)ДяВЛЕНЪЕбщФПЕФЕФЪЧ(ЁЁЁЁ )ЁЃ
ЁЁ ЁЁAЃЎFeCl2ШмвК(KSCNШмвК)ЁЁЁЁЁЁЁЁ BЃЎKIШмвК(ЕэЗлШмвК)
ЁЁ ЁЁCЃЎHCHOШмвК(зЯЩЋЪЏШяЪдвК)ЁЁ ЁЁЁЁDЃЎK2SO3ШмвК(BaCl2ШмвК)
[НтЮі]бЁDЁЃAЯюЃЌШєFeCl2ШмвКБЛбѕЛЏЃЌШмвКжаЛсгаFe3+ЩњГЩЃЌМгШыKSCNШмвККѓШмвКБфКьЩЋЃЛBЯюЃЌKIШмвКБЛбѕЛЏЃЌШмвКжаЛсгаI2ЩњГЩЃЌМгШыЕэЗлШмвККѓШмвКБфРЖЃЛCЯюЃЌHCHOШмвКБЛбѕЛЏЃЌШмвКжаЛсгаHCOOHЩњГЩЃЌМгШызЯЩЋЪЏШяЪдвКШмвКБфКьЩЋЃЛDЯюЃЌЮоТлK2SO3ШмвКЪЧЗёБЛбѕЛЏЃЌМгШыBaCl2ШмвККѓЖМгаАзЩЋГСЕэЩњГЩЁЃ
8ЃЎ(2010ЁЄЯЬбєФЃФт)ИљОнS2O82Ѓ+2eЃЁњ2SO42ЃЁЂMn2++4H2OЁњMnO4Ѓ+8H++5eЃЃЌЭЦВтбѕЛЏ1.5mol Mn2+ашS2O82ЃЕФЮяжЪЕФСПЮЊ(ЁЁЁЁ )ЁЃ
ЁЁ AЃЎ1.5molЁЁ ЁЁBЃЎ3.75molЁЁ ЁЁCЃЎ3.25molЁЁЁЁ DЃЎ3.125mol
[НтЮі]бЁBЁЃИљОнбѕЛЏЛЙдЗДгІЕУЪЇЕчзгЪ§ЯрЕШЃЌПЩвдЕУШчЯТЙиЯЕЪНЃК5S2O82Ѓ~10eЃ~2Mn2+ЃЌЫљвдn(S2O82Ѓ)ЃН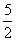 n(Mn2+)ЃН
n(Mn2+)ЃН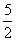 ЁС1.5molЃН3.75molЁЃ
ЁС1.5molЃН3.75molЁЃ
7ЃЎ(2010ЁЄКЃПкФЃФт)вбжЊМИжжвѕРызгЛЙдадЧПШѕЫГађЮЊOHЃЃМClЃЃМBrЃЃМIЃЃМS2ЃЁЃШєФГШмвККЌгаЯрЭЌХЈЖШЕФOHЃЁЂClЃЁЂBrЃЁЂIЃЁЂS2ЃЃЌЕБЯђЦфжаж№ЕЮМгШыаТжЦЕФБЅКЭТШЫЎжБжСЙ§СПЪБЃЌзюКѓБЛбѕЛЏЕФРызгЪЧ(ЁЁЁЁ )ЁЃ
ЁЁ AЃЎBrЃ ЁЁЁЁЁЁBЃЎClЃЁЁ ЁЁЁЁCЃЎOHЃЁЁ ЁЁЁЁDЃЎS2Ѓ
[НтЮі]бЁAЁЃвђЮЊЛЙдадЃКS2ЃЃОIЃЃОBrЃЃОClЃЃОOHЃЃЌЫљвдCl2ЯШИњЛЙдадзюЧПЕФ
S2ЃЗЂЩњжУЛЛЗДгІЩњГЩSЕЅжЪЃЌШЛКѓдйгыIЃЗЂЩњжУЛЛЗДгІЩњГЩI2ЕЅжЪЃЌзюКѓКЭBrЃЗЂЩњжУЛЛЗДгІЩњГЩBr2ЕЅжЪЁЃЬиБ№зЂвтCl2ВЛФмНЋClЃКЭOHЃбѕЛЏЃЌЗёдђЛсДэбЁCЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com