
科目:高中化学 来源:2007-2008学年山东省济宁市高三(上)期末化学试卷(解析版) 题型:选择题

科目:高中化学 来源:2011-2012学年江苏省苏州五中高一第二学期期中考试化学试卷(带解析) 题型:实验题
(10分)下表是某城市某日的空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
科目:高中化学 来源:2014届江苏省高一第二学期期中考试化学试卷(解析版) 题型:实验题
(10分)下表是某城市某日的空气质量报告:
|
污染指数 |
首要污染物 |
空气质量级别 |
空气质量状况 |
|
55 |
SO2 |
II |
良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
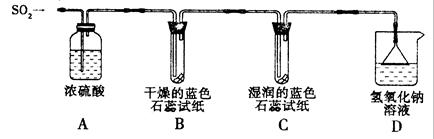
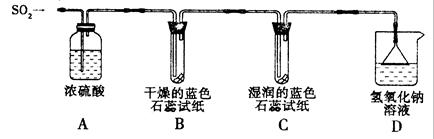
[探究实验一]用下图所示装置进行实验。
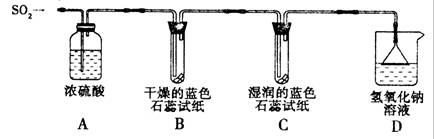
① A装置的作用是 (填“干燥”或“氧化”)SO2气体。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变 色,说明SO2与水反应生成一种酸。
③ D装置的作用是 ,D中发生反应的化学方程式是 。
[探究实验二]往盛有水的烧杯中通入SO2气体,测得所得溶液的pH 7(填“>”“=”或“<”),然后每隔1 h测定其pH,发现pH逐渐 (填“变大”或“变小”),直至恒定。说明烧杯中的溶液被空气中的氧气氧化最终生成H2SO4。
[查阅资料]SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4。则在此过程中的飘尘是作为 (填“催化剂”或“氧化剂”)。
[探究结论]SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
[知识拓展]
(1)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为 ,是造成酸雨的另一主要原因。
(2)该市某工厂的燃料煤中硫的质量分数为0.16%,该工厂每天燃烧这种煤100吨。如果煤中的硫全部转化为SO2,那么这些SO2在标准状况下的体积约为 m3。
科目:高中化学 来源:不详 题型:实验题
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
科目:高中化学 来源: 题型:阅读理解
 某化学实验小组用右图所示的装置制取乙酸乙酯,并检验乙 酸 乙 酯中是否含有乙酸杂质(铁架台、夹子等支撑仪器省略).已知乙酸乙酯的沸点为77.1℃,乙醇沸点为78.4℃,乙酸的沸点为118℃.请根据要求填空:
某化学实验小组用右图所示的装置制取乙酸乙酯,并检验乙 酸 乙 酯中是否含有乙酸杂质(铁架台、夹子等支撑仪器省略).已知乙酸乙酯的沸点为77.1℃,乙醇沸点为78.4℃,乙酸的沸点为118℃.请根据要求填空: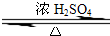 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O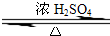 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O科目:高中化学 来源:同步题 题型:实验题
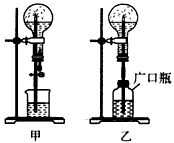
(2)利用甲装置实验,还有哪些试剂可以形成喷泉_________
A.CO和NaOH溶液 B.O2和NaOH溶液 C.SO2和NaOH溶液 D.CO2和盐酸溶液
(3)某同学积极思考后,设计了如图乙的装置,也同样形成了喷泉。已知该同学在广口瓶中装入的是稀硫酸和另一种固体物质,待它们反应完全后,打开止水夹,在上方的烧瓶内也形成喷泉。该同学加入的固体物质可能是__________
A.铜片 B.碳酸钠粉末 C.锌粒 D.熟石灰
(4)比较甲、乙两套装置,从产生喷泉的原理来分析,甲装置是___(用“增大”或“减小”填空,下同)上部烧瓶内气体压强;乙装置是___下部广口瓶内气体压强。
(5)城市中常见的人造喷泉以及自然界的火山爆发原理与上述___(填“甲”或“乙”)装置的原理相似。
科目:高中化学 来源:2011-2012学年山西省高三第一次阶段性诊断考试化学试卷 题型:实验题
(10分)某课外活动小组对污染大气的部分非金属氧化物进行探究。请根据题目要求回答下列问题:
(1) 写出用铜与稀硝酸反应制取一氧化氮的离子方程式: ________________
(2)查阅资料得知: 。实验室有如图所示的装置.则制取一氧化碳可选用的装置为________________(填字母)。
。实验室有如图所示的装置.则制取一氧化碳可选用的装置为________________(填字母)。

(3)汽车尾气是当前城市大气污染的主要来源之一.汽车尾气中的主要污染物为一氧化碳和氮氧化物。汽车尾气催化转化装置可将这些有害气体转化为无害物质。该小组设计了如图所示的装置(部分夹持装置已略去).在实验室模拟汽车尾气处理的过程。

①实验前关闭K2,打开K1从K1处先通氮气排净装置中的空气,其目的是________
②装置III内发生反应的化学方程式为________
③实验过程中,装置V内可观察到的现象是________________
④实验结束后,关闭K1,停止加热,打开K2,通入适量空气后,装置IV中可观察到有红棕色气体生成.该气体是________________(填化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com