
肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )
 |
科目:高中化学 来源: 题型:
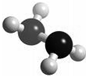 肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )
肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )科目:高中化学 来源:不详 题型:单选题
| A.肼是由极性键和非极性键构成的非极性分子 |
| B.肼沸点高达l13℃,可推测肼分子间可形成氢键 |
| C.肼燃烧的热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-642 kJ?mol-1 |
| D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH- |

科目:高中化学 来源:2009年江苏省宿迁市泗阳县致远中学高考化学模拟试卷(二)(解析版) 题型:选择题
科目:高中化学 来源:2012届新疆乌鲁木齐一中高三第三次月考化学试卷 题型:单选题
肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如图所示,下列有关说法正确的是( )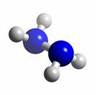
| A.肼是由极性键和非极性键构成的非极性分子 |
| B.肼沸点高达l13℃,可推测肼分子间能形成氢键 |
| C.肼燃烧的热化学方程式为:N2H4(g)+ O2(g) = N2(g) +2H2O(g);△H = -642 kJ·mol-1 |
| D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH- |
科目:高中化学 来源:2011-2012学年新疆乌鲁木齐一中高三第三次月考化学试卷 题型:选择题
肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如图所示,下列有关说法正确的是( )
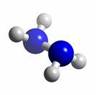
A、肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间能形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+ O2(g) = N2(g) +2H2O(g);△H = -642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH-
科目:高中化学 来源:不详 题型:单选题

| A.肼是由极性键和非极性键构成的非极性分子 |
| B.肼沸点高达l13℃,可推测肼分子间能形成氢键 |
| C.肼燃烧的热化学方程式为:N2H4(g)+ O2(g) = N2(g) +2H2O(g);△H = -642 kJ·mol-1 |
| D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH- |
科目:高中化学 来源: 题型:单选题

科目:高中化学 来源: 题型:
肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如图所示,下列有关说法正确的是( )
A、肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间能形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+ O2(g) = N2(g) +2H2O(g);△H = -642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH-
科目:高中化学 来源: 题型:
肼(N2H4)是航天飞船常用的高能燃料,肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642 kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如下图所示,下列有关说法正确的是 ( )

A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-642kJ?mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH-
科目:高中化学 来源:2013-2014学年山东省济宁市高三第一次模拟理综化学试卷(解析版) 题型:填空题
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂。请回答下列问题:
(1)已知:N2(g) + 2O2(g) == 2NO2(g)????????????????? ΔH= + 67.7kJ·mol-1
N2H4(g) + O2(g)== N2(g) + 2H2O(g)????? ΔH= - 534.0kJ·mol-1
2NO2(g)  N2O4(g)????????????? ΔH= - 52.7kJ·mol-1
N2O4(g)????????????? ΔH= - 52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:?????????????????????????????????? ;
(2)工业上用次氯酸钠与过量的氨气反应制备肼,该反应的化学方程式为:???????????????????????????????????? ;
(3)工业上可以用下列反应原理制备氨气:
2N2(g)+6H2O(l) 4NH3(g)+3O2(g)?? ΔH= Q kJ·mol-1
4NH3(g)+3O2(g)?? ΔH= Q kJ·mol-1
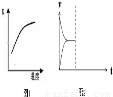
①已知该反应的平衡常数K与温度的关系如图,则此反应的 Q ?????? 0 (填“>”“<”或“=”)。
②若起始加入氮气和水,15分钟后,反应达到平衡,此时NH3的浓度为0.3mol/L,则用氧气表示的反应速率为??????????? 。
③常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, ???????? (选填编号).
A.容器中气体的平均相对分子质量不随时间而变化????
B.v(N2)/v(O2)=2∶3
C.容器中气体的密度不随时间而变化
D.通入稀有气体能提高反应的速率
E.若向容器中继续加入N2,N2的转化率将增大
(4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。
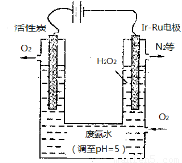
①为不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+) ?????? c(NO3-)(填“>”“<”或“=”);
②Ir—Ru惰性电极有吸附O2作用,该电极的电极反应为????????????????????? ;
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为???????????? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com