
вбжЊжаКЭШШЕФЪ§жЕЪЧ57.3kJ?mol-1ЃЎЯТСаЮяжЪЗДгІЪБЃЌВњЩњ57.3kJШШСПЕФЪЧЃЈЁЁЁЁЃЉ
|
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂЯЁHClКЭЯЁNaOH | BЁЂ1.0mol?L-1 HClКЭ1.0mol?L-1 NaOH | CЁЂ500mL 2.0 mol?L-1 HClКЭ500mL2.0mol?L-1 NaOH | DЁЂ500mL 2.0 mol?L-1 H2SO4КЭ500mL 2.0mol?L-1 BaЃЈOHЃЉ2 |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎЯЁHClКЭЯЁNaOH |
| BЃЎ1.0mol?L-1HClКЭ1.0mol?L-1NaOH |
| CЃЎ500mL2.0mol?L-1HClКЭ500mL2.0mol?L-1NaOH |
| DЃЎ500mL2.0mol?L-1H2SO4КЭ500mL2.0mol?L-1BaЃЈOHЃЉ2 |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2011-2012бЇФъдЦФЯЪЁЕТКъжнТКЮїЪаУЂЪажабЇИпвЛЃЈЯТЃЉЦкФЉЛЏбЇЪдОэЃЈЮФПЦЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2011-2012бЇФъСЩФўЪЁЩђбєЖўжаИпвЛЯТбЇЦкЦкжаПМЪдЛЏбЇЪдОэЃЈДјНтЮіЃЉ ЬтаЭЃКЪЕбщЬт
ЃЈ8ЗжЃЉгУвЛЖЈХЈЖШЕФЯЁбЮЫсгыЯЁNaOHШмвКдкзѓЯТЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЃЌЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃвбжЊЧПЫсгыЧПМюЕФжаКЭШШЮЊ57.3KJ/molЃЌЫЎЕФБШШШШнЮЊ4.2J/(gЁЄЁц)ЃЌгаЙиШШСПгыБШШШШнЕФМЦЫуЙЋЪНЃКQ=mЁСcЁСЁїtЃЈQЮЊШШСПЃЌmЮЊЮяжЪЕФжЪСПЃЌcЮЊБШШШШнЃЌЁїtЮяжЪЮТЖШЕФБфЛЏжЕЃЉ
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉДгЪЕбщзАжУЩЯПДЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇгУЦЗЪЧЃК
ЃЈ2ЃЉНЋV1 mL 1.0 mol/L HClШмвККЭV2 mLЮДжЊХЈЖШЕФNaOHШмвКЛьКЯОљдШКѓВтСПВЂМЧТМШмвКЮТЖШЃЌЪЕбщНсЙћШчЭМЫљЪО(ЪЕбщжаЪМжеБЃГжV1ЃЋV2ЃН50 mL)ЁЃ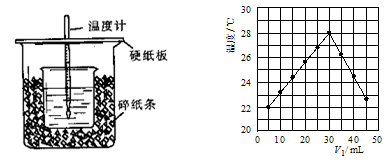
ЯТСаа№Ъіе§ШЗЕФЪЧ
| AЃЎзіИУЪЕбщЪБЛЗОГЮТЖШЮЊ22 Ёц | BЃЎИУЪЕбщБэУїЛЏбЇФмПЩвдзЊЛЏЮЊШШФм |
| CЃЎNaOHШмвКЕФХЈЖШдМЪЧ1.00 mol/L | DЃЎИУЪЕбщБэУїгаЫЎЩњГЩЕФЗДгІЖМЪЧЗХШШЗДгІ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014НьСЩФўЪЁИпвЛЯТбЇЦкЦкжаПМЪдЛЏбЇЪдОэЃЈНтЮіАцЃЉ ЬтаЭЃКЪЕбщЬт
ЃЈ8ЗжЃЉгУвЛЖЈХЈЖШЕФЯЁбЮЫсгыЯЁNaOHШмвКдкзѓЯТЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЃЌЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃвбжЊЧПЫсгыЧПМюЕФжаКЭШШЮЊ57.3KJ/molЃЌЫЎЕФБШШШШнЮЊ4.2J/(gЁЄЁц)ЃЌгаЙиШШСПгыБШШШШнЕФМЦЫуЙЋЪНЃКQ=mЁСcЁСЁїtЃЈQЮЊШШСПЃЌmЮЊЮяжЪЕФжЪСПЃЌcЮЊБШШШШнЃЌЁїtЮяжЪЮТЖШЕФБфЛЏжЕЃЉ
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉДгЪЕбщзАжУЩЯПДЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇгУЦЗЪЧЃК
ЃЈ2ЃЉНЋV1 mL 1.0 mol/L HClШмвККЭV2 mLЮДжЊХЈЖШЕФNaOHШмвКЛьКЯОљдШКѓВтСПВЂМЧТМШмвКЮТЖШЃЌЪЕбщНсЙћШчЭМЫљЪО(ЪЕбщжаЪМжеБЃГжV1ЃЋV2ЃН50 mL)ЁЃ
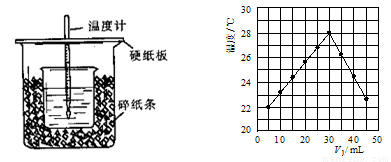
ЯТСаа№Ъіе§ШЗЕФЪЧ
AЃЎзіИУЪЕбщЪБЛЗОГЮТЖШЮЊ22 Ёц BЃЎИУЪЕбщБэУїЛЏбЇФмПЩвдзЊЛЏЮЊШШФм
CЃЎNaOHШмвКЕФХЈЖШдМЪЧ1.00 mol/L DЃЎИУЪЕбщБэУїгаЫЎЩњГЩЕФЗДгІЖМЪЧЗХШШЗДгІ
ЃЈ3ЃЉV1=30mLЪБHClКЭNaOHЧЁКУЗДгІЃЌИљОнЬтжаЫљИјЪ§ОнЫуГіЕФЮТЖШБфЛЏжЕдМЮЊ
ЃЈБЃСєећЪ§ЃЌМЦЫуЪБПЩНЋЯЁШмвКЕФУмЖШМАБШШШШнПДГЩгыЫЎНќЫЦЯрЭЌЃЌЧвШмвКЛьКЯЪБЬхЛ§БфЛЏКіТдВЛМЦЃЉЃЛЖјИљОнЩЯЭМЕФЮТЖШБфЛЏПЩЖСГіЮТЖШБфЛЏжЕдМ7 ЁцЃЛСНепЯрБШЫљВтНсЙћЦЋЕЭЃЌдьГЩШчДЫЯжЯѓЕФдвђгаЃК
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
гУвЛЖЈХЈЖШЕФЯЁбЮЫсгыЯЁNaOHШмвКдкзѓЯТЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЃЌЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃвбжЊЧПЫсгыЧПМюЕФжаКЭШШЮЊ57.3KJ/molЃЌЫЎЕФБШШШШнЮЊ4.2J/(gЁЄЁц)ЃЌгаЙиШШСПгыБШШШШнЕФМЦЫуЙЋЪНЃКQ=mЁСcЁСЁїtЃЈQЮЊШШСПЃЌmЮЊЮяжЪЕФжЪСПЃЌcЮЊБШШШШнЃЌЁїtЮяжЪЮТЖШЕФБфЛЏжЕЃЉ
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉДгЪЕбщзАжУЩЯПДЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇгУЦЗЪЧЃК
ЃЈ2ЃЉНЋV1 mL 1.0 mol/L HClШмвККЭV2 mLЮДжЊХЈЖШЕФNaOHШмвКЛьКЯОљдШКѓВтСПВЂМЧТМШмвКЮТЖШЃЌЪЕбщНсЙћШчЭМЫљЪО(ЪЕбщжаЪМжеБЃГжV1ЃЋV2ЃН50 mL)ЁЃ
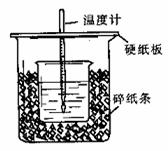
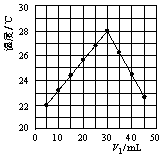
ЯТСаа№Ъіе§ШЗЕФЪЧ
AЃЎзіИУЪЕбщЪБЛЗОГЮТЖШЮЊ22 Ёц BЃЎИУЪЕбщБэУїЛЏбЇФмПЩвдзЊЛЏЮЊШШФм
CЃЎNaOHШмвКЕФХЈЖШдМЪЧ1.00 mol/L DЃЎИУЪЕбщБэУїгаЫЎЩњГЩЕФЗДгІЖМЪЧЗХШШЗДгІ
ЃЈ3ЃЉV1=30mLЪБHClКЭNaOHЧЁКУЗДгІЃЌИљОнЬтжаЫљИјЪ§ОнЫуГіЕФЮТЖШБфЛЏжЕдМЮЊ
ЃЈБЃСєећЪ§ЃЌМЦЫуЪБПЩНЋЯЁШмвКЕФУмЖШМАБШШШШнПДГЩгыЫЎНќЫЦЯрЭЌЃЌЧвШмвКЛьКЯЪБЬхЛ§БфЛЏКіТдВЛМЦЃЉЃЛЖјИљОнЩЯЭМЕФЮТЖШБфЛЏПЩЖСГіЮТЖШБфЛЏжЕдМ7 ЁцЃЛСНепЯрБШЫљВтНсЙћЦЋЕЭЃЌдьГЩШчДЫЯжЯѓЕФдвђгаЃК
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЪЕбщЬт

| AЃЎзіИУЪЕбщЪБЛЗОГЮТЖШЮЊ22 Ёц | BЃЎИУЪЕбщБэУїЛЏбЇФмПЩвдзЊЛЏЮЊШШФм |
| CЃЎNaOHШмвКЕФХЈЖШдМЪЧ1.00 mol/L | DЃЎИУЪЕбщБэУїгаЫЎЩњГЩЕФЗДгІЖМЪЧЗХШШЗДгІ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2010-2011бЇФъеуНЪЁеђКЃжабЇИпШ§бЇФъФЃФтОэвЛЛЏбЇЪдОэЃЈРэзлЃЉЃЈ5дТЗнЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКНтД№Ьт
| ШѕЫс | CH3COOH | H2SO3 | HCN |
| ЮяжЪЕФСПХЈЖШmol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
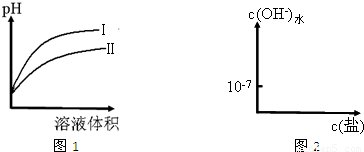
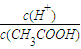 ЭЌЪБдіДѓЕФЪЧ______ЃЎ
ЭЌЪБдіДѓЕФЪЧ______ЃЎ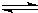 H+ЃЈaqЃЉ+CN-ЃЈaqЃЉЁїH=+43.5kJ?mol-1
H+ЃЈaqЃЉ+CN-ЃЈaqЃЉЁїH=+43.5kJ?mol-1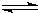 HCNЃЈaqЃЉ+OH-ЃЈaqЃЉЕФЁїH=______ЃЎИУЗДгІ25ЁцЪБЕФЦНКтГЃЪ§K=______ЃЎ
HCNЃЈaqЃЉ+OH-ЃЈaqЃЉЕФЁїH=______ЃЎИУЗДгІ25ЁцЪБЕФЦНКтГЃЪ§K=______ЃЎПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЮЪД№Ьт
| ШѕЫс | CH3COOH | H2SO3 | HCN |
| ЮяжЪЕФСПХЈЖШmol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
| c(H+) |
| c(CH3COOH) |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com