
已知碳酸、亚硫酸、次氯酸的平衡常数如下表:
|
科目:高中化学 来源:沈阳二模 题型:单选题
| H2CO3 | H2SO3 | HClO |
| K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A.NaClO溶液中通少量CO2:2ClO-+CO2+H2O=2HClO+CO32- |
| B.Na2CO3溶液中通少量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- |
| C.NaHCO3溶液中通少量SO2:2HCO3-+SO2=CO2+SO32-+H2O |
| D.NaClO溶液中通少量SO2:2ClO-+SO2+H2O=2HClO+SO32- |
科目:高中化学 来源:2010年辽宁省沈阳市高考化学二模试卷(解析版) 题型:选择题
| H2CO3 | H2SO3 | HClO |
| K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
科目:高中化学 来源:专项题 题型:单选题

[ ]
科目:高中化学 来源: 题型:
(2010?沈阳二模)已知碳酸、亚硫酸、次氯酸的平衡常数如下表:
|
科目:高中化学 来源:2013届辽宁省沈阳二中高三第四次阶段测试化学试卷(带解析) 题型:单选题
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如右表,下列叙述正确的是
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
科目:高中化学 来源:2012年天津市河东区高考化学一模试卷(解析版) 题型:选择题
| 酸 | 电离平衡常数 |
| 醋酸 | Ki=1.75×10-5 |
| 次氯酸 | Ki=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
科目:高中化学 来源:不详 题型:单选题
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
科目:高中化学 来源: 题型:单选题
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
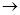 SO32— + 2HClO
SO32— + 2HClO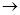 HCO3— + HClO
HCO3— + HClO科目:高中化学 来源:不详 题型:单选题
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
 SO32— + 2HClO
SO32— + 2HClO HCO3— + HClO
HCO3— + HClO科目:高中化学 来源:2012-2013学年辽宁省高三第四次阶段测试化学试卷(解析版) 题型:选择题
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如右表,下列叙述正确的是
|
酸 |
电离平衡常数 |
|
醋酸 |
K i=1.75×10-5 |
|
次氯酸 |
K i=2.98×10-8 |
|
碳酸 |
Ki1=4.30×10-7 Ki2=5.61×10-11 |
|
亚硫酸 |
Ki1=1.54×10-2 Ki2=1.02×10-7 |
A.将0.1mol/L的醋酸加水不断稀释,c(CH3COO—)始终减小
B少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO—==CO32—+2HClO
C.少量的反应的离子方程式为:SO2+H2O+Ca2++2ClO—==CaSO3↓+2HClO
D.25℃,等浓度的CH3COONa、NaClO、Na2CO3和Na2SO3 溶液中,碱性最强的是Na2CO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com