
中学化学中涉及到一些重要的化学工业,以下有关化工生产叙述正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.氯气通入到饱和的石灰水中可制得大量漂粉精 | ||||
| B.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来 | ||||
C.工业上,用SiO2+2C
| ||||
| D.接触法制H2SO4在接触室中SO2氧化条件一般选择高温、高压、催化剂 |
科目:高中化学 来源:不详 题型:单选题
| A.氯气通入到饱和的石灰水中可制得大量漂粉精 | ||||
| B.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来 | ||||
C.工业上,用SiO2+2C
| ||||
| D.接触法制H2SO4在接触室中SO2氧化条件一般选择高温、高压、催化剂 |
科目:高中化学 来源:2011年河南省洛阳市宜阳实验中学高考一轮复习化学试卷(二)(解析版) 题型:选择题
 Si+2CO↑制得粗硅
Si+2CO↑制得粗硅科目:高中化学 来源: 题型:单选题
 Si+2CO↑制得粗硅
Si+2CO↑制得粗硅科目:高中化学 来源: 题型:
| A、工业上,用焦炭在高温下还原二氧化硅制得粗硅 | B、通常将氯气通入到饱和石灰水中制得大量漂白粉 | C、工业制硫酸将SO2氧化成SO3的条件一般选择高温、高压、催化剂 | D、钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来 |
科目:高中化学 来源:2013-2014学年山东省泰安市高三第一轮复习质量检测化学试卷(解析版) 题型:选择题
工业生产中常涉及到一些重要的中学化学反应,以下有关叙述正确的是
A.工业上,用焦炭在高温下还原二氧化硅制得粗硅
B.通常将氯气通入到饱和石灰水中制得大量漂白粉
C.工业制硫酸将 氧化成
氧化成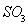 的条件一般选择高温、高压、催化剂
的条件一般选择高温、高压、催化剂
D.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来
科目:高中化学 来源: 题型:单选题
工业生产中常涉及到一些重要的中学化学反应,以下有关叙述正确的是
| A.工业上,用焦炭在高温下还原二氧化硅制得粗硅 |
| B.通常将氯气通入到饱和石灰水中制得大量漂白粉 |
C.工业制硫酸将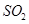 氧化成 氧化成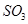 的条件一般选择高温、高压、催化剂 的条件一般选择高温、高压、催化剂 |
| D.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来 |
科目:高中化学 来源:不详 题型:单选题
| A.工业上,用焦炭在高温下还原二氧化硅制得粗硅 |
| B.通常将氯气通入到饱和石灰水中制得大量漂白粉 |
C.工业制硫酸将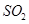 氧化成 氧化成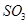 的条件一般选择高温、高压、催化剂 的条件一般选择高温、高压、催化剂 |
| D.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来 |
科目:高中化学 来源: 题型:

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com