
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )
|
科目:高中化学 来源:2012-2013学年北京市某重点中学高二(上)期末化学试卷(解析版) 题型:选择题

科目:高中化学 来源:2012-2013学年江苏省无锡市江阴市祝塘中学高二(上)期中化学试卷(解析版) 题型:选择题

科目:高中化学 来源:2013-2014学年山东省烟台市高三上学期期末统考化学试卷(解析版) 题型:填空题
某蓄电池反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。
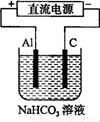
(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:

已知:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
开始沉淀时的pH |
2.3 |
7.5 |
5.6 |
6.2 |
|
完全沉淀时的pH |
3.9 |
9.7 |
6.4 |
8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
科目:高中化学 来源: 题型:填空题
某蓄电池反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |


| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
科目:高中化学 来源: 题型:
右图是铜锌原电池,某同学做完实验后记录如下:
 ①Zn为正极,Cu为负极 ②电解质溶液pH不变 ③电子流动的方向为:Zn→Cu
①Zn为正极,Cu为负极 ②电解质溶液pH不变 ③电子流动的方向为:Zn→Cu
④Cu极上有氢气产生 ⑤若有1mol电子流过导线,则产生氢气0.5 mol
⑥该原电池产生氢气的速度比没有导线相连时慢
上述记录中描述正确的是
A.①②③ B.①②⑥ C.③④⑤ D.④⑤⑥
科目:高中化学 来源: 题型:
(10分)右下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)在卡片上,叙述合理的是__________________(填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是____________________________________________________。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因________________。
(4)如果把硫酸换成硫酸铜溶液,猜测_________(填“锌极”或“铜极”)变粗,原因是__________________(用电极方程式表示)。
科目:高中化学 来源:2013届浙江省宁波市高一下学期期末化学试卷 题型:填空题
(10分)右下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:

(1)在卡片上,叙述合理的是__________________(填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是____________________________________________________。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因________________。
(4)如果把硫酸换成硫酸铜溶液,猜测_________(填“锌极”或“铜极”)变粗,原因是__________________(用电极方程式表示)。
科目:高中化学 来源: 题型:
右下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
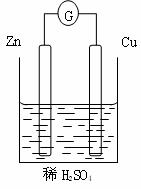
| Date:2011.03.06 实验后的记录: ①Zn为阳极,Cu为阴极 ②H+向负极移动 ③电子流动方向Zn→Cu ④Cu极有H2产生 ⑤若有1mol电子流过导线,则产生H2为0.5mol。 ⑥正极的电极反应式:Zn-2e- =Zn2+ |
(1)在卡片上,叙述合理的是__________________(填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是____________________________________________________。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因________________。
(4)如果把硫酸换成硫酸铜溶液,猜测_________(填“锌极”或“铜极”)变粗,原因是__________________(用电极方程式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com