
¸ůľÝ±íÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇŁ¨ˇˇˇˇŁ©
|
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁşµĄŃˇĚâ
¸ůľÝ±íÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇŁ¨ Ł©
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | | ClŁ |
| ˘Ú | KMnO4 | H2O2 | H2SO4 | O2 | Mn2Ł« |
| ˘Ű | KClO3 | ŨŃÎËá | / | Cl2 | |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş2016˝ě˝Î÷ʡŇË´şĘиßŇ»ÉĎѧĆÚĆÚÖĐżĽĘÔ»ŻŃ§ĘÔľíŁ¨˝âÎö°ćŁ© ĚâĐÍŁşŃˇÔńĚâ
¸ůľÝ±íÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇŁ¨ Ł©
ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
˘Ů | Cl2 | FeBr2 | / |
| ClŁ |
˘Ú | KMnO4 | H2O2 | H2SO4 | O2 | Mn2Ł« |
˘Ű | KClO3 | ŨŃÎËá | / | Cl2 |
|
AŁ®±íÖТŮ×é·´Ó¦żÉÄÜÓĐŇ»ÖÖ»ňÁ˝ÖÖÔŞËر»Ńő»Ż
BŁ®Ńő»ŻĐÔÇżČő±Č˝ĎŁşKClO3>Fe3Ł«>Cl2>Br2
CŁ®±íÖТÚ×é·´Ó¦µÄŔë×Ó·˝łĚĘ˝ĘÇ2MnO4-Ł«3H2O2Ł«6HŁ«=2Mn2Ł«Ł«4O2ˇüŁ«6H2O
DŁ®±íÖТŰ×é·´Ó¦µÄ»ąÔ˛úÎďĘÇKClŁ¬µç×ÓתŇĆĘýÄżĘÇ6eŁ
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş2011-2012ѧÄę±±ľ©ĘĐĘŻľ°É˝Çř¸ßČýŁ¨ÉĎŁ©ĆÚÄ©»ŻŃ§ĘÔľíŁ¨˝âÎö°ćŁ© ĚâĐÍŁşŃˇÔńĚâ
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | Cl- | |
| ˘Ú | KClO3 | ŨŃÎËá | / | Cl2 | |
| ˘Ű | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş2012-2013ѧÄę±±ľ©ĘĐͨÖÝÇřÓŔŔÖµęÖĐѧ¸ßČýŁ¨ÉĎŁ©ĆÚÖĐ»ŻŃ§ĘÔľíŁ¨˝âÎö°ćŁ© ĚâĐÍŁşŃˇÔńĚâ
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | Cl- | |
| ˘Ú | KClO3 | ŨŃÎËá | / | Cl2 | |
| ˘Ű | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | Cl- | |
| ˘Ú | KClO3 | ŨŃÎËá | / | Cl2 | |
| ˘Ű | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| Aˇ˘±íÖТŮ×éµÄ·´Ó¦Ö»żÉÄÜÓĐŇ»ÖÖÔŞËر»Ńő»ŻşÍŇ»ÖÖÔŞËر»»ąÔ |
| Bˇ˘Ńő»ŻĐÔÇżČőµÄ±Č˝ĎŁşKClO3ŁľFe3+ŁľCl2ŁľBr2 |
| Cˇ˘ÓɱíÖТ٢Ú×é·´Ó¦ÍƲ⣺ClO3-ˇ˘Br-ˇ˘H+ˇ˘Fe2+˛»ÄÜÔÚŨČÜŇşÖĐ´óÁżą˛´ć |
| Dˇ˘±íÖТŰ×é·´Ó¦µÄŔë×Ó·˝łĚʽΪŁş2MnO4-+3H2O2+6H+¨T2Mn2++4O2ˇü+6H2O |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş˛»Ďę ĚâĐÍŁşµĄŃˇĚâ
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | Cl- | |
| ˘Ú | KClO3 | ŨŃÎËá | / | Cl2 | |
| ˘Ű | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| AŁ®±íÖТŮ×éµÄ·´Ó¦żÉÄÜÓĐŇ»ÖÖ»ňÁ˝ÖÖÔŞËر»Ńő»Ż |
| BŁ®Ńő»ŻĐÔÇżČőµÄ±Č˝ĎŁşKClO3ŁľFe3+ŁľCl2ŁľBr2 |
| CŁ®±íÖТÚ×é·´Ó¦µÄ»ąÔ˛úÎďĘÇKClŁ¬µç×ÓתŇĆĘýÄżĘÇ6e- |
| DŁ®±íÖТŰ×é·´Ó¦µÄŔë×Ó·˝łĚʽΪŁş2MnO4-+3H2O2+6H+=2Mn2++4O2ˇü+6H2O |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
Ł¨2013?ł¤´şŇ»ÄŁŁ©¸ůľÝ±íÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇŁ¨ˇˇˇˇŁ©
|
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş˛»Ďę ĚâĐÍŁşµĄŃˇĚâ
| ĐňşĹ | Ńő»ŻĽÁ | »ąÔĽÁ | ĆäËű·´Ó¦Îď | Ńő»Ż˛úÎď | »ąÔ˛úÎď |
| ˘Ů | Cl2 | FeBr2 | / | Cl- | |
| ˘Ú | KClO3 | ŨŃÎËá | / | Cl2 | |
| ˘Ű | KMnOo | e2O2 | e2ÁůOo | O2 | Mn2+ |
| AŁ®±íÖТŮ×éµÄ·´Ó¦Ö»żÉÄÜÓĐŇ»ÖÖÔŞËر»Ńő»ŻşÍŇ»ÖÖÔŞËر»»ąÔ |
| BŁ®Ńő»ŻĐÔÇżČőµÄ±Č˝ĎŁşKClO3ŁľFe3+ŁľCl2ŁľBr2 |
| CŁ®ÓɱíÖТ٢Ú×é·´Ó¦ÍƲ⣺ClO3-ˇ˘Br-ˇ˘H+ˇ˘Fe2+˛»ÄÜÔÚŨČÜŇşÖĐ´óÁżą˛´ć |
| DŁ®±íÖТŰ×é·´Ó¦µÄŔë×Ó·˝łĚʽΪŁş2MnO4-+3H2O2+6H+¨T2Mn2++4O2ˇü+6H2O |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ϱíÎŞ˛ż·Ö¶ĚÖÜĆÚÔŞËصÄÔ×Ӱ뾶Ľ°ĆäÖ÷ŇŞ»ŻşĎĽŰŁ¬
|
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş2012-2013ѧÄęÉ˝¶«ĘˇĽĂÄĎĘиßČý4ÔÂą®ąĚĐÔѵÁ·Ŕí×Ű»ŻŃ§ĘÔľíŁ¨˝âÎö°ćŁ© ĚâĐÍŁşĽĆËăĚâ
ÁňÔŞËصĻŻşĎÎďÔÚÉú˛úˇ˘Éú»îÖĐÓĐ×Ĺąă·şµÄÓ¦ÓáŁ
Ł¨1Ł©400ˇćŁ¬1.01ˇÁ PaĎÂŁ¬ČÝ»ýÎŞ1Ł®0LµÄĂܱŐČÝĆ÷ÖĐłäČë0.5molSO2,
(g)şÍ0.3 molO2 (g)Ł¬·˘Éú·´Ó¦2SO2(g)Ł«O2(g)
PaĎÂŁ¬ČÝ»ýÎŞ1Ł®0LµÄĂܱŐČÝĆ÷ÖĐłäČë0.5molSO2,
(g)şÍ0.3 molO2 (g)Ł¬·˘Éú·´Ó¦2SO2(g)Ł«O2(g)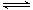 2SO3(g)
ˇ÷HŁ˝Ł198kJ/molˇŁ·´Ó¦ÖĐn(SO3)şÍn(O2)ËćʱĽä±ä»ŻµÄąŘϵČçÓŇÍĽËůĘľ
2SO3(g)
ˇ÷HŁ˝Ł198kJ/molˇŁ·´Ó¦ÖĐn(SO3)şÍn(O2)ËćʱĽä±ä»ŻµÄąŘϵČçÓŇÍĽËůĘľ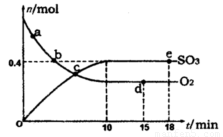 ˇŁ·´Ó¦µÄĆ˝şâłŁĘýKŁ˝_______Ł»0µ˝10 minÄÚÓĂSO2±íĘľµÄĆ˝ľů·´Ó¦ËŮÂĘ_________ˇŁ¸ůľÝÍĽÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇ_____Ł¨ĚîĐňşĹŁ©ˇŁ
ˇŁ·´Ó¦µÄĆ˝şâłŁĘýKŁ˝_______Ł»0µ˝10 minÄÚÓĂSO2±íĘľµÄĆ˝ľů·´Ó¦ËŮÂĘ_________ˇŁ¸ůľÝÍĽÖĐĐĹϢŁ¬ĹжĎĎÂÁĐĐđĘöÖĐŐýČ·µÄĘÇ_____Ł¨ĚîĐňşĹŁ©ˇŁ
AŁ®aµăʱżĚµÄŐý·´Ó¦ËŮÂʱČbµăʱżĚµÄ´ó
BŁ®cµăʱżĚ·´Ó¦´ďµ˝Ć˝şâ״̬
CŁ®dµăşÍeµăʱżĚµÄc(O2)Ďŕͬ
DŁ®Čô5 00ˇćŁ¬1.01ˇÁ105PaĎÂŁ¬·´Ó¦´ďµ˝Ć˝şâʱŁ¬n( SO3) ±ČÍĽÖĐeµăʱżĚµÄÖµ´ó
Ł¨2Ł©ÓĂNaOHČÜŇşÎüĘŐą¤Ňµ·ĎĆřÖеÄSO2Ł¬µ±ÎüĘŐҺʧȥÎüĘŐÄÜÁ¦Ę±Ł¬25ˇćʱ˛âµĂČÜŇşµÄpH=5.6Ł¬ČÜŇşÖĐNaŁ«,HŁ«, HSO3Ł,SO32ŁŔë×ÓµÄŨ¶ČÓÉ´óµ˝ĐˇµÄËłĐňĘÇ__________________ˇŁ
Ł¨3Ł©żÉͨąýµç˝â·¨ĘąŁ¨2Ł©ÖеÄÎüĘŐŇşÔŮÉú¶řŃ»·ŔűÓĂŁ¨µçĽ«ľůÎŞĘŻÄ«µçĽ«Ł©Ł¬Ć乤×÷ĘľŇâÍĽČçĎÂŁş

HSO3ŁÔÚŃôĽ«ĘŇ·´Ó¦µÄµçĽ«·´Ó¦Ę˝ÎŞ________________________Ł¬ŇőĽ«ĘҵIJúÎď_________________ˇŁ
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com