
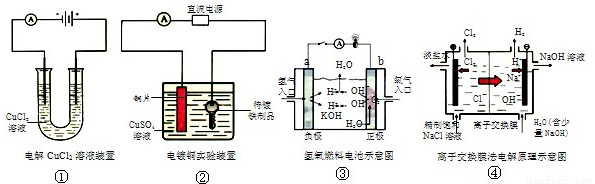
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法不正确的是( )
|
科目:高中化学 来源: 题型:
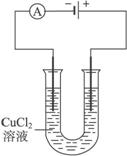
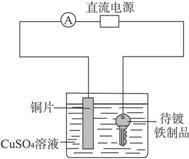
①电解CuCl2溶液装置 ②电镀铜实验装置
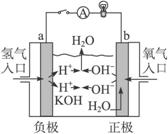
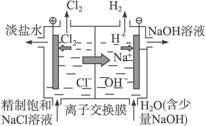
③氢氧燃料电池示意图 ④离子交换膜法电解原理示意图
(1)写出装置①中发生反应的总化学方程式__________________________________。
(2)装置②中铜片为______极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2 mol电子转移,此时铜片和铁制品的质量差为____________g。
(3)装置③中b极为______极,该极的电极反应方程式为_________________。
(4)装置④为工业上电解食盐水制取NaOH的原理示意图,其中阳离子交换膜将电解槽隔成阳极室和阴极室,阳极室加入精制的饱和食盐水,阴极室加入纯水(含一定量的NaOH)。
请解释阴极的纯水中加入NaOH的原因:__________________________________________。
科目:高中化学 来源: 题型:
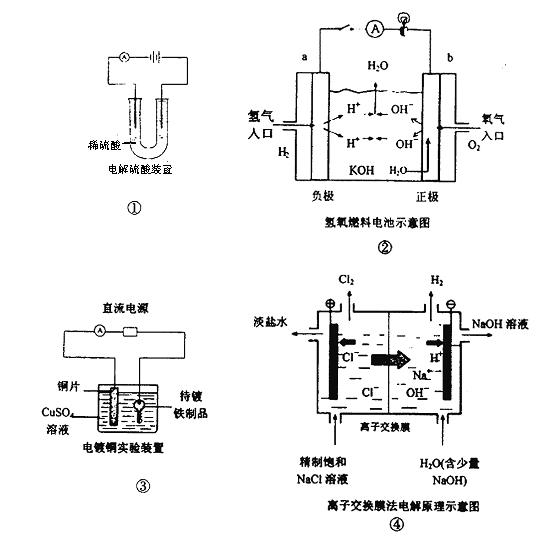
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是

A. 装置①中电解一段时间后,溶液的PH不变。
B. 装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O
C. 装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol
电子转移,此时铜片和铁制品的质量差为128g
D. 装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2
科目:高中化学 来源:2011年浙江省台州市路桥中学高考化学模拟试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:不详 题型:单选题

| A.装置①中正极反应式为:2Cl--2e-=Cl2,负极反应式为:Cu2++2e-=Cu |
| B.装置②中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g |
| C.装置③中b极为正极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
| D.装置④阴极的纯水中加入NaOH的作用是:增大离子浓度,增强溶液的导电性 |
科目:高中化学 来源:不详 题型:单选题
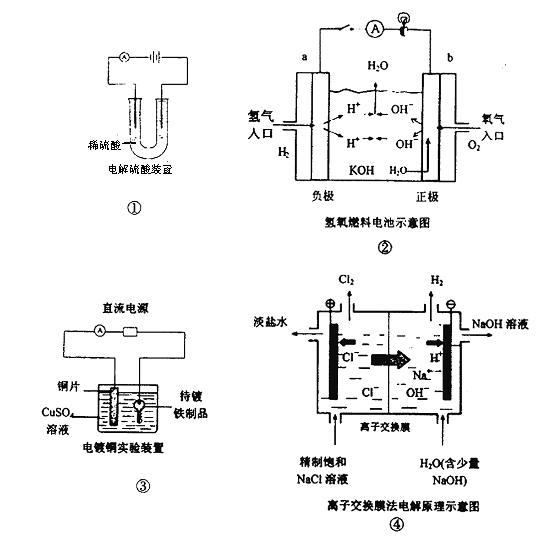
| A.装置①中电解一段时间后,溶液的PH不变。 |
| B.装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O |
| C.装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol 电子转移,此时铜片和铁制品的质量差为128g |
| D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com