
能使H2O?H++OHˉ电离平衡向正反应方向移动,而且所得溶液显酸性的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.将水加热到99℃,使水的pH=6.1 |
| B.在水中滴入稀H2SO4 |
| C.在水中加入Na2CO3固体 |
| D.在水中加入氯化铝固体 |
科目:高中化学 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(B)(解析版) 题型:选择题
科目:高中化学 来源: 题型:
能使H2O ![]() H++ OHˉ电离平衡向正反应方向移动,而且所得溶液显酸性的是
H++ OHˉ电离平衡向正反应方向移动,而且所得溶液显酸性的是
A.将水加热到99℃,使水![]() 的pH=6.1 B.在水中滴入稀H2SO4
的pH=6.1 B.在水中滴入稀H2SO4
C.在水中加入Na2CO3固体 D.在水中加入氯化铝固体
科目:高中化学 来源:三点一测丛书 高中化学(选修)化学反应原理 江苏版课标本 江苏版课标本 题型:021
|
能使H2O+H2O | |
A. |
在水中加入NaHCO3 |
B. |
在水中加入CuCl2 |
C. |
在水中加入稀硫酸 |
D. |
将水加热到99℃(其中c(H+)=10-6 mol/L) |
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +H2O
+H2O![]() NH3·H2O+H+ ②
NH3·H2O+H+ ②
H++OH-![]() H2O ③
H2O ③
由于![]() 水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +OH-
+OH-![]() NH3·H2O ②
NH3·H2O ②
由于NH4Cl电离出的![]() 与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是_________(填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)你说明丙同学做出该选择的理由:______________________________。
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理_____________(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式_____________________________________。
科目:高中化学 来源: 题型:解答题
科目:高中化学 来源:同步题 题型:填空题
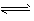 Mg2++2OH-①
Mg2++2OH-① 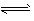 NH3·H2O+H+②
NH3·H2O+H+②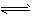 H2O③
H2O③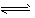 Mg2++2OH-①
Mg2++2OH-①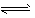 NH3·H2O②
NH3·H2O② 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com