
| A、B、C、D分别为固体氧化物燃料电池、碱性燃料电池、质子交换膜燃料电池、熔融盐燃料电池,其中正极的反应产物为水的是 ( )
|
科目:高中化学 来源:不详 题型:单选题
A. | B. | C. | D. |
科目:高中化学 来源:2009-2010学年山东省济南市高三(上)期末化学试卷(解析版) 题型:选择题
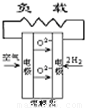
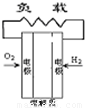
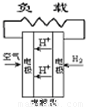
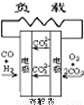
科目:高中化学 来源: 题型:
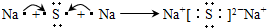
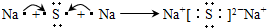
| ||
| ||
科目:高中化学 来源: 题型:


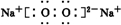
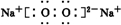
科目:高中化学 来源: 题型:
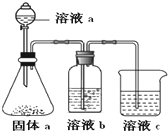 A、B、C、D、E、F是周期表中短周期的六种元素,有关性质或结构信息如下表:
A、B、C、D、E、F是周期表中短周期的六种元素,有关性质或结构信息如下表:| 元素 | 有关性质或结构信息 |
| A | 雷雨天大气中会有A的一种单质生成 |
| B | B离子与A离子电子数相同,且是所在周期中单核离子半径最小的 |
| C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
| D | D是制造黑火药的一种成分,也可用于杀菌消毒 |
| E | E与D同周期,且在该周期中原子半径最小 |
| F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
科目:高中化学 来源: 题型:
?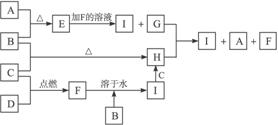
1)四种物质的名称:B__________,C___________,H____________,G_______________;
(2)物质I溶液的颜色呈_______________色,物质A的颜色是_________________色;
(3)B物质在化学反应中,与强氧化剂反应通常生成______价的化合物,与较弱氧化剂反应通常生成____________价的化合物;
(4)用实验方法鉴别H和I可用___________试剂,现象是_______________,并写出由H制取I的化学方程式________________________;
(5)G+H→I+A+F的离子方程式________________________________________________。
科目:高中化学 来源: 题型:
分别取它们的溶液进行实验,主要操作及现象如下:
①向A的溶液中通入二氧化碳,再加入品红溶液,红色褪去。
②将B和C的溶液混合,生成白色沉淀,该沉淀可溶于E溶液。
③将B和D的溶液混合,生成白色沉淀,继续加入过量的E溶液,有气泡产生的同时还有白色沉淀存在。
④A和E溶液的焰色反应都呈黄色。
(1)写出下列物质的化学式:A_________、C_________、D_________。
(2)写出A—E溶液中,与铝发生置换反应的离子方程式为_____________________________
(3)向B的溶液中,缓慢滴入少量稀的E溶液,其主要的离子方程式为__________________
科目:高中化学 来源: 题型:
①向A的溶液中通入二氧化碳,再加入品红溶液,红色褪去。
②A、B、E的溶液的焰色反应都呈黄色
③将B和C的溶液混合,生成白色沉淀,该沉淀可溶于E溶液
④将B和D的溶液混合,生成白色沉淀,继续加入过量的E溶液,有气泡产生的同时还有白色沉淀存在。
(1)写出下列物质的化学式:A________________________,C_____________________。
(2)向B的溶液中,缓慢滴入少量的E溶液,其主要的离子方程式为__________________
________________________________________。
科目:高中化学 来源: 题型:
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。
请回答下列问题:
(1)B、D在周期表中同处在_____族,D的原子结构示意图是 ,下列可以验证B与D两元素原子得电子能力强弱的实验事实是 (填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的原子的电子层数
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢化合的难易
(2)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式 ;
(3)A、B、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有l0个电子,则甲与乙反应的离子方程式为 ;
(4)D元素的气态氢化物和其低价氧化物能反应生成D的单质.该反应中氧化产物与还原产物的物质的量之比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com