
已知反应H2+I2═2HI,在一定条件下的数据如下,根据数据判断该反应是( )
|
科目:高中化学 来源: 题型:
已知反应H2+I2═2HI,在一定条件下的数据如下,根据数据判断该反应是( )
|
科目:高中化学 来源:不详 题型:单选题
| 化 学 键 | H-H | I-I | H-I |
| 断开时吸收的能量或形成时放出的能量(kJ/mol) | 436 | 151 | 299 |
| A.放热反应 | B.吸热反应 |
| C.没有热量变化 | D.无法判断 |
科目:高中化学 来源:2011-2012学年北京市重点中学高一(下)期中化学试卷(解析版) 题型:选择题
| 化 学 键 | H-H | I-I | H-I |
| 断开时吸收的能量或形成时放出的能量(kJ/mol) | 436 | 151 | 299 |
科目:高中化学 来源: 题型:
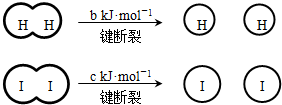 (a、b、c均大于零)
(a、b、c均大于零)| A、反应物的总能量高于生成物的总能量 | B、断开1mol H-H键和1mol I-I键所需能量大于断开2mol H-I键所需能量 | C、断开2mol H-I键所需能量约为(c+b+a)kJ | D、向密闭容器中加入2mol H2和2mol I2,充分反应后放出的热量小于2a kJ |
科目:高中化学 来源:2013-2014学年北京市海淀区高三上学期期末考试化学试卷(解析版) 题型:选择题
H2和I2在一定条件下能发生反应:H2(g) +I2(g)
 2HI(g)
△H=—a kJ·mol-1
2HI(g)
△H=—a kJ·mol-1
已知: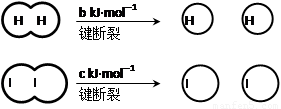 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
A.反应物的总能量高于生成物的总能量
B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C.断开2 mol H-I键所需能量约为(c+b+a) kJ
D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
科目:高中化学 来源: 题型:单选题
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
科目:高中化学 来源:不详 题型:单选题
 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1 (a、b、c均大于零)
(a、b、c均大于零)| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
科目:高中化学 来源: 题型:
 动(填“向左”、“向右”或“不”).
动(填“向左”、“向右”或“不”).科目:高中化学 来源:2013-2014学年山东省青岛市高三3月第一次模拟考试(第二套)理综化学试卷(解析版) 题型:填空题
液氨常用作制冷剂,回答下列问题
(1)一定条件下在密闭容器中发生反应:
a.NH4I(s) NH3(g) + HI(g)?????? b.2HI(g)
NH3(g) + HI(g)?????? b.2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
①写出反应a的平衡常数表达式??????????????????
②达到平衡后,扩大容器体积,反应b的移动方向?????? (填“正向”、“逆向”或“不移动”),达到新的平衡时容器内颜色将怎样变化?????? (填“加深”、“变浅”或“不变”)
(2)工业上合成氨的反应:N2(g)+3H2(g)  2NH3(g)? ΔH=-92.60 kJ·mol-1
2NH3(g)? ΔH=-92.60 kJ·mol-1
下列说法能说明上述反应向正反应方向进行的是________(填序号)。
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N—H键的同时生成2n mol H—H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(3)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
???????????????? 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0 | 0.20 |
| 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2 h时放出的热量为________ kJ。
②0~1 h内N2的平均反应速率为________ mol·L-1·h-1。
③此温度下该反应的化学平衡常数K=________(保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________方向移动(填“正反应”或“逆反应”)。
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱在溶液中分步电离,请用离子反应方程式表示其水溶液显碱性的原因????????????????????????
科目:高中化学 来源: 题型:填空题
液氨常用作制冷剂,回答下列问题
(1)一定条件下在密闭容器中发生反应:
a.NH4I(s)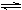 NH3(g) + HI(g) b.2HI(g)
NH3(g) + HI(g) b.2HI(g) 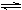 H2(g) + I2(g)
H2(g) + I2(g)
①写出反应a的平衡常数表达式
②达到平衡后,扩大容器体积,反应b的移动方向 (填“正向”、“逆向”或“不移动”),达到新的平衡时容器内颜色将怎样变化 (填“加深”、“变浅”或“不变”)
(2)工业上合成氨的反应:N2(g)+3H2(g) 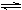 2NH3(g) ΔH=-92.60 kJ·mol-1
2NH3(g) ΔH=-92.60 kJ·mol-1
下列说法能说明上述反应向正反应方向进行的是________(填序号)。
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N—H键的同时生成2n mol H—H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(3)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | | 1.00 | 1.00 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com