
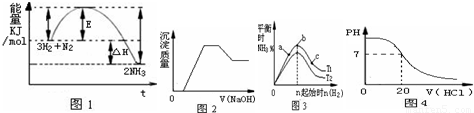
有关下列图象说法正确的是( )
|
科目:高中化学 来源:2012-2013学年湖南省岳阳一中高三(上)第一次质检化学试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题

| A.由图1可知合成氨反应为自发反应,加入适当的催化剂,E和△H都减小 |
| B.图2表示向含有H+、Mg2+、Al3+、NH4+中加入NaOH溶液与产生沉淀质量的变化关系 |
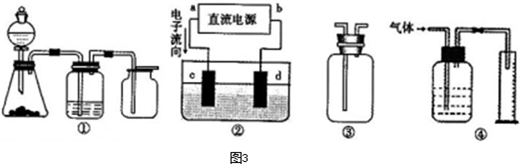
| C.图3表示合成氨反应在其他条件不变的情况下,改变起始物n(H2)对此反应平衡的影响.可知反应物N2的转化率最高的是b点;T1>T2,K2>K1(T1和T2表示温度,K1、K2表示对应温度下平衡常数) |
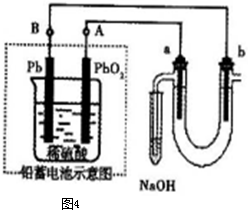
| D.图4表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1氨水的pH随加入盐酸体积的变化 |
科目:高中化学 来源: 题型:
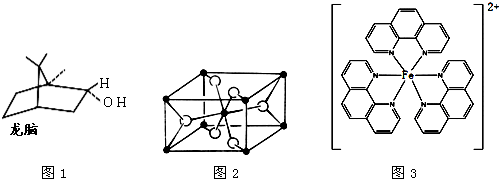
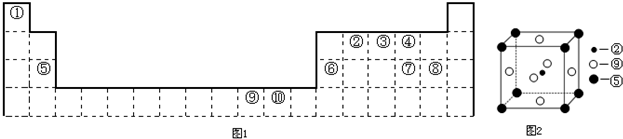
 ),它能与Fe2+形成红色配合物(如图3),该配离子中Fe2+配位数为
),它能与Fe2+形成红色配合物(如图3),该配离子中Fe2+配位数为科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:阅读理解


| ||
| 8d3 |
| ||
| 8d3 |
科目:高中化学 来源: 题型:
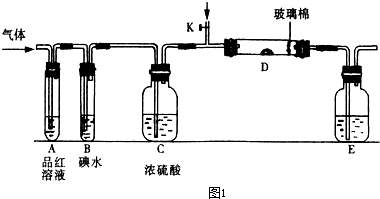
硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
![]()
①写出由纯SiHCl3制备高纯硅的化学反应方程式 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式 ;H2还原SiHCl3过程中若混O2,可能引起的后果是 。
(2)下列有关硅材料的说法正确的是 (填字母)。
A.碳化硅化学性质稳定,可用于生产耐高温水混
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.普通玻璃是由纯碱、石灰石和石英砂的,其熔点很高
D.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。写出实验现象并给予解释 。
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |

科目:高中化学 来源: 题型:
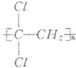 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由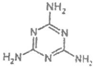
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com