
已知0.1mol?L-1的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,要使溶液中
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水.
|
科目:高中化学 来源: 题型:
| c(H+) |
| c(CH3COOH) |
科目:高中化学 来源:不详 题型:单选题
| c(H+) |
| c(CH3COOH) |
| A.①② | B.①③ | C.②④ | D.③④ |
科目:高中化学 来源:2011-2012学年甘肃省嘉峪关一中高二(上)期末化学试卷(解析版) 题型:选择题
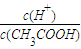 的值增大,可以采取的措施是( )
的值增大,可以采取的措施是( )科目:高中化学 来源:2012-2013年黑龙江哈尔滨第十二中学高二上学期期末考试化学试卷(带解析) 题型:填空题
水溶液中存在多种平衡,请回答下列问题。
(1)有下列几种溶液:a. NH3·H2O b. CH3COONa c. NH4Cl d. NaHSO4
常温下呈酸性的溶液有 (填序号)。
(2)已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、
,该溶液中的离子浓度由大到小的顺序是: 。
(3)有浓度均为0.1 mol?L-1的 ①盐酸②硫酸③醋酸三种溶液,请用序号填空:
三种溶液的c(H+)大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH的大小关系为 。
(4)25℃时,AgCl的Ksp=1.8×10-10 ,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化)。
科目:高中化学 来源:2014届黑龙江哈尔滨第十二中学高二上学期期末考试化学试卷(解析版) 题型:填空题
水溶液中存在多种平衡,请回答下列问题。
(1)有下列几种溶液:a. NH3·H2O b. CH3COONa c. NH4Cl d. NaHSO4
常温下呈酸性的溶液有 (填序号)。
(2)已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、
,该溶液中的离子浓度由大到小的顺序是: 。
(3)有浓度均为0.1 mol?L-1的 ①盐酸②硫酸③醋酸三种溶液,请用序号填空:
三种溶液的c(H+)大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH的大小关系为 。
(4)25℃时,AgCl的Ksp=1.8×10-10 ,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化)。
科目:高中化学 来源:不详 题型:填空题
科目:高中化学 来源: 题型:
| c(CH3COO-)?c(H+) | c(CH3COOH) |
科目:高中化学 来源: 题型:阅读理解
(11分)碘是人体的必需微量元素之一。加碘食盐中加重主的碘酸钾是一种白色结晶粉末,常温下很稳定。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物等还原性物质反应。
I.工业生产碘碳钾的流程如下:
|
已知步骤①发生反应为6I2+11KclO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑
反应中还原剂是 (填化学式),转移电子数为 。
II、已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(1)检验加碘食物中的碘元素。
学生甲利用碘酸与碘化钾在酸性条件下发生反应,检验是否有碘单质生成所需要的试剂是 ,判断碘单质存在的现象是 ;若要进一步分离提纯碘单质,用到的主要玻璃仪器有 。
(2)测定加碘食盐中碘的含量。学生乙设计的实验步骤如下:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Ns2S2O3溶液10.0mL,恰好完全反应(I2+2S2O2-3=2I-+S4O2-6)。则加碘食盐样品中的碘元素含量是 mg./kg(以含w的代数式表示)。
(3)有人认为可以用碘化钾代替食盐中的碘酸钾,学生丙又进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液。 | 溶液无变化 |
| 滴入5滴淀粉溶液和1ml0.1mol/L KI溶液,振荡。 | 溶液无变化 |
| 然后再加入少量食醋,振荡。 | 溶液变蓝色 |
根据学生丙的实验结果,回答下列问题
①你认为能否用碘化钾代替食盐中的碘酸钾 (填“能、不能或不确定”)②你认为学生乙的实验结果 (填“偏高、偏低、无影响”)。
科目:高中化学 来源: 题型:
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH ![]() CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)25 ℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是 ;
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(2)25 ℃时,在 pH =5的稀醋酸溶液中,c(CH3COO-)= (填数字表达式);
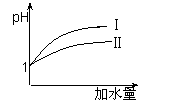 (3)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水
(3)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水
量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化
的曲线是 ;
(4)25 ℃时,向体积为Va mLpH=3的醋酸溶液中滴加pH=11的
NaOH溶液Vb mL至溶液恰好呈中性,则Va与的Vb关系是
Va Vb(填“>”、“<”或“=”)。
(5)25 ℃时,若向氨水中加入稀盐酸至溶液的pH=7,此时[NH4+]=a mol/L,
则[Cl-]=________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com